Obésité : Que se passe-t-il après l’arrêt des incrétino-mimétiques ?

En 2022, 38% de la population mondiale (soit 2.6 milliards de personnes) étaient soit en surpoids ou souffraient d’obésité, conditions qui augmentent le risque de morbidité et de mortalité prématurée. Les incrétino-mimétiques, médicaments de gestion du poids qui regroupent les agonistes du GLP-1, les agonistes du GIP et les agonistes combinés GLP-1/GIP, occupent aujourd’hui une place centrale dans la prise en charge de l’obésité. Ils ont profondément modifié le paysage thérapeutique, avec des pertes de masse corporelle de l’ordre de 15 à 20% de leur masse initiale. Ces résultats ont suscité un enthousiasme légitime, tant chez les professionnels de santé que chez les patients, en laissant entrevoir une alternative pharmacologique efficace là où les approches comportementales (diète et activité physique) seules peinaient souvent à produire des effets durables.
Mais l’obésité est une maladie chronique, marquée par des mécanismes biologiques puissants de défense du poids corporel. La question clé n’est donc pas uniquement de savoir si ces traitements font perdre du poids, mais ce qu’il advient une fois le traitement interrompu. Or, dans la pratique, l’arrêt des médicaments est fréquent, que ce soit pour des raisons de tolérance, de coût, de disponibilité ou d’adhésion à long terme. Il est estimé qu’une personne sur deux arrête ce traitement en l’espace d’une année. Comprendre la dynamique pondérale après l’arrêt de ces traitements, et comment elle évolue en comparaison à celle observée après l’arrêt de programmes comportementaux classiques, est donc essentiel pour évaluer leur véritable impact sur la santé à long terme.
L’étude réalisée
Pour cela, des chercheurs de l’université d’Oxford ont mené une revue systématique et une méta-analyse portant sur l’ensemble des études disponibles ayant évalué l’évolution de la masse corporelle après l’arrêt du traitement médicamenteux chez des adultes en surpoids ou obèses. Les bases de données biomédicales majeures ont été interrogées depuis leur création jusqu’à début 2025, sans restriction de date ou de langue, afin d’identifier des essais randomisés, des essais non randomisés et des études observationnelles pertinentes.
Pour être incluses, les études devaient comporter une phase de traitement médicamenteux d’au moins huit semaines, suivie d’une période de suivi sans médicament d’au moins quatre semaines. Les molécules étudiées couvraient un large spectre, allant des traitements plus anciens comme l’orlistat ou la sibutramine, jusqu’aux mimétiques d’incrétine récentes telles que le sémaglutide ou le tirzépatide. Au total, trente-sept études, représentant soixante-trois bras d’intervention et 9341 participants, ont été intégrées à l’analyse. Parmi ces études 35 étaient des essais randomisés contrôlés et 28 études possédaient un groupe contrôle à la fois durant l’intervention et le suivi.
Les auteurs ont utilisé plusieurs modèles statistiques complémentaires pour estimer la trajectoire de reprise pondérale dans le temps, en exprimant les résultats sous forme de taux mensuels moyens. Ils ont également analysé l’évolution des marqueurs cardiométaboliques après l’arrêt du traitement, et comparé ces dynamiques à celles observées après l’arrêt de programmes comportementaux de gestion du poids, issus de travaux antérieurs menés par la même équipe.
Résultats & Analyses
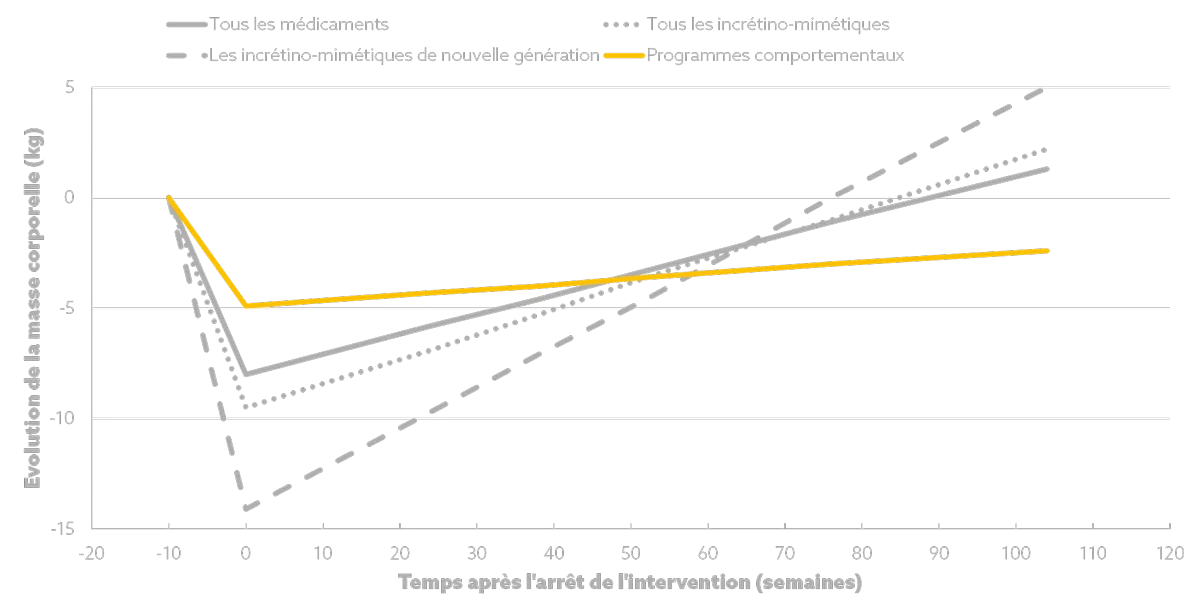
Les principaux résultats montrent que l’arrêt des médicaments incrétino-mimétiques est suivi, en moyenne, d’une reprise de poids rapide et progressive, avec un taux moyen de 0.4 kg par mois. Cette reprise survient quel que soit le type de médicament utilisé, y compris les molécules les plus récentes et les plus efficaces pendant la phase de traitement. La trajectoire observée suggère que le poids corporel tendrait à revenir vers sa valeur initiale en l’espace de 1.7 années après l’arrêt du traitement.
Mais cette dynamique ne concerne pas uniquement le poids. Les améliorations cardiométaboliques obtenues pendant la phase de perte de poids suivent une trajectoire parallèle. Ainsi, après l’arrêt du traitement, l’hémoglobine glyquée (HbA1C), la glycémie à jeun, le cholestérol, les triglycérides et la pression artérielle (diastolique et systolique) évoluent progressivement vers leurs valeurs de départ, pour y revenir en 1.4 années, suggérant que les bénéfices cardiométaboliques sont étroitement dépendants du maintien de la perte pondérale induite par le médicament.
Les auteurs de l’étude précisent également que les données étaient insuffisantes pour analyser les changements dans les marqueurs cardiométaboliques après un traitement avec des mimétiques de l’incrétine plus récents et plus efficaces (une seule étude avec un suivant de 2 ans après l’arrêt d’un traitement avec semaglutide, par exemple), mais ils montrent tout de même que la reprise de poids est plus rapide (0,8 kg/mois) et qu’un retour au poids initial est prévu 1.5 an après l’arrêt du traitement, ce qui implique que les bénéfices sur la santé cardiovasculaire s’atténueront probablement aussi plus rapidement.
Un élément particulièrement intéressant est la comparaison avec les programmes comportementaux. Bien que les médicaments permettent en moyenne une perte de poids plus importante, plus rapidement, la reprise pondérale après leur arrêt est plus rapide que celle observée après la fin de programmes basés sur l’alimentation et l’activité physique. De plus, les bénéfices cardiométaboliques durent au moins 5 ans après l’arrêt du programme. Cette différence persiste même après ajustement sur l’ampleur de la perte de poids initiale, ce qui suggère que la nature de l’intervention, et pas seulement le poids perdu, influence la capacité à maintenir les bénéfices dans le temps.
Ces résultats s’inscrivent dans une logique physiologique cohérente. Les médicaments amaigrissants agissent principalement en modifiant les signaux de faim et de satiété, rendant le comportement alimentaire plus facile à contrôler tant que le traitement est présent. Une fois ce soutien pharmacologique retiré, les mécanismes biologiques de défense du poids reprennent le dessus, en l’absence de stratégies comportementales durablement intégrées.
Applications pratiques
Ces données invitent à une réflexion plus large sur la place des médicaments dans la prise en charge de l’obésité. Elles ne remettent pas en cause leur efficacité à court terme, ni leur intérêt dans certaines situations cliniques. En revanche, elles soulignent les limites d’une utilisation ponctuelle ou de courte durée, sans stratégie globale visant le maintien des adaptations à long terme. L’obésité étant une affection chronique et récidivante, un traitement prolongé par incrétino-mimétiques peut être nécessaire pour maintenir les bénéfices pour la santé. Un essai a montré que le traitement continu par semaglutide permettait de maintenir la perte de poids pendant quatre ans. Toutefois, aux États-Unis et au Danemark, les premières données montrent que les taux d’abandon en dehors des essais cliniques sont d’environ 50% à un an. Ces données suggèrent que malgré leur succès dans la perte de poids initiale, ces médicaments seuls peuvent ne pas être suffisants pour contrôler le poids à long terme.
De plus, ces résultats rappellent que la perte de poids induite par un médicament ne constitue pas une “réinitialisation” durable du système de régulation du poids. Sans accompagnement prolongé, sans modifications comportementales consolidées, et sans réflexion sur la durée réelle du traitement, la probabilité d’un effet rebond est élevée. Cela ne signifie pas que ces traitements sont inutiles, mais qu’ils doivent être envisagés comme un outil parmi d’autres, et non comme une solution autonome.
Pour les professionnels de santé, les conclusions de cette étude renforcent l’importance de discuter dès l’initiation du traitement de ce qui se passera après. Pour les patients, elles permettent de poser des attentes réalistes : le médicament facilite la perte de poids, mais ne remplace ni le travail de fond sur les habitudes de vie, ni la nécessité d’un suivi à long terme. Les auteurs de l’étude expliquent d’ailleurs qu’une enquête menée auprès d’adultes américains a révélé que 45% d’entre eux étaient intéressés par l’utilisation d’agonistes du récepteur du GLP-1 pour la gestion du poids, mais cette proportion tombe à 14% lorsque les personnes sont informées de la reprise de poids après l’arrêt du traitement.
Référence
West S, Scragg J, Aveyard P, Oke JL, Willis L, Haffner SJP, Knight H, Wang D, Morrow S, Heath L, Jebb SA & Koutoukidis DA. Weight regain after cessation of medication for weight management: systematic review and meta-analysis. BMJ 2026, 392 : e085304.