Le tissu adipeux et son dysfonctionnement dans l’obésité

Longtemps relégué au rôle de simple réserve de graisse, le tissu adipeux est désormais reconnu comme un organe dynamique, complexe et endocrine jouant un rôle central dans la régulation du métabolisme énergétique et de nombreuses fonctions physiologiques. Le corps humain stocke de l’énergie sous forme de triglycérides dans les adipocytes (les cellules adipeuses) afin de disposer d’une réserve calorique mobilisable en cas de besoin. Cependant, loin d’être inerte, le tissu adipeux communique avec les autres organes par le biais d’hormones et de cytokines (appelées adipokines), modulant ainsi l’appétit, la dépense énergétique, la sensibilité à l’insuline et même les réponses immunitaires.
Il existe plusieurs types de tissu adipeux aux propriétés distinctes, de la graisse blanche stockant l’énergie à la graisse brune dissipant de l’énergie sous forme de chaleur. Ces dépôts adipeux sont répartis dans différentes régions du corps, et cette répartition influence fortement la santé métabolique : la graisse localisée autour des viscères n’a pas les mêmes effets que celle située sous la peau. De plus, le tissu adipeux fait preuve d’une remarquable plasticité. Il peut changer de taille, de structure cellulaire et de fonction en réponse aux conditions de l’organisme, comme par exemple lors d’une prise de poids, d’une exposition au froid ou d’une grossesse. Cette capacité d’adaptation, ou remodelage, est au cœur de son fonctionnement sain mais aussi de son dérèglement.
En effet, dans des conditions pathologiques comme l’obésité (caractérisée par un excès chronique de calories stockées en graisse), le tissu adipeux peut perdre sa capacité d’adaptation et devenir dysfonctionnel. Un tissu adipeux “malade” se traduit par des adipocytes surchargés et stressés, un état inflammatoire chronique, une fibrose tissulaire et des sécrétions hormonales altérées. Ces dysfonctionnements contribuent directement aux complications de l’obésité telles que la résistance à l’insuline, le diabète de type 2, la stéatose hépatique non alcoolique ou les maladies cardiovasculaires. À l’inverse, la préservation d’un tissu adipeux sain et fonctionnel apparaît comme un facteur de protection, il est d’ailleurs possible de parler d’obésité métaboliquement saine chez certains individus dont le tissu adipeux, bien que surabondant, parvient à se remodeler sans induire de troubles métaboliques majeurs (au moins pendant un certain temps).
Face à l’épidémie mondiale d’obésité, comprendre le fonctionnement du tissu adipeux est un enjeu scientifique et médical crucial. Ce dossier propose une synthèse critique des connaissances actuelles concernant les différents types de tissu adipeux et leur distribution, la plasticité adipocytaire et ses mécanismes, les fonctions endocrines de cet organe, ainsi que les dérèglements du tissu adipeux observés dans l’obésité. Nous aborderons également les implications cliniques de ces notions et les pistes thérapeutiques émergentes. L’objectif est d’offrir une compréhension claire et nuancée du rôle du tissu adipeux dans la santé métabolique, en mettant en lumière les principaux modèles explicatifs, les résultats convergents ou contradictoires des recherches, et les questions qui restent ouvertes.
Les différents types de tissu adipeux
Tous les tissus adipeux ne se valent pas : il en existe plusieurs types, définis par leur composition cellulaire, leur localisation et leurs fonctions spécifiques. On distingue classiquement le tissu adipeux blanc, le tissu adipeux brun et une forme intermédiaire qualifiée de tissu adipeux beige. Chacun joue un rôle particulier dans l’organisme.

Adipocyte blanc 
Adipocyte brun 
Adipocyte beige
Tissu adipeux blanc
Le tissu adipeux blanc est le plus abondant chez l’adulte. C’est à lui que l’on fait généralement référence lorsqu’on parle de “graisse corporelle”. Il est constitué majoritairement d’adipocytes blancs, cellules de grande taille (50 à 150 µm de diamètre) contenant une unique gouttelette lipidique volumineuse qui occupe l’essentiel de l’espace cellulaire. Cette morphologie dite uniloculaire est adaptée à la fonction principale du tissu adipeux blanc : stocker les triglycérides pendant les périodes d’excédent énergétique, puis les libérer sous forme d’acides gras lorsque le corps en a besoin (jeûne, exercice prolongé, exposition au froid). L’adipocyte blanc est ainsi une cellule spécialisée dans le stockage d’énergie et la lipolyse (dégradation des graisses) sur demande.
Au-delà de ce rôle de réservoir calorique, le tissu adipeux blanc est un organe endocrine important. Il sécrète en continu de nombreuses molécules signal appelées adipokines, qui vont agir localement ou à distance sur le cerveau, le foie, les muscles, le système immunitaire, etc. Parmi les hormones produites par la graisse blanche figurent la leptine (qui informe le cerveau des réserves énergétiques et tend à diminuer l’appétit) et l’adiponectine (qui augmente la sensibilité à l’insuline et exerce des effets anti-inflammatoires et cardioprotecteurs). Le tissu adipeux blanc produit également des cytokines pro-inflammatoires (TNF-α, IL-6…), en partie via les cellules immunitaires résidentes, surtout lorsque les adipocytes sont hypertrophiés. Nous reviendrons plus loin en détail sur ces fonctions endocrines. Notons simplement ici que le tissu adipeux blanc, loin d’être un tissu passif, communique avec l’ensemble de l’organisme et contribue activement à l’homéostasie métabolique.
Chez un adulte en bonne santé, la graisse blanche représente la majeure partie de la masse grasse totale et se situe principalement sous la peau (graisse sous-cutanée) et autour des organes abdominaux (graisse viscérale). On la retrouve également dans d’autres emplacements spécifiques (orbites, paumes, plante des pieds, etc.) où elle sert de coussin de protection mécanique. En résumé, le tissu adipeux blanc est le site principal de stockage lipidique de l’organisme et un acteur endocrine majeur. Il assure un équilibre énergétique en stockant l’énergie excédentaire et en la redistribuant selon les besoins, tout en envoyant des signaux hormonaux sur l’état des réserves.
Tissu adipeux brun
Le tissu adipeux brun est un type de graisse bien différent, spécialisé dans la production de chaleur plutôt que dans le stockage. Il tire son nom de sa couleur brunâtre due à sa richesse en mitochondries (organites cellulaires contenant du fer, d’où la couleur brune). Les adipocytes bruns sont de plus petite taille que les blancs et contiennent de multiples petites gouttelettes lipidiques (morphologie multiloculaire). Surtout, ils expriment en grande quantité une protéine mitochondriale unique appelée UCP1 (uncoupling protein 1) ou thermogénine, qui court-circuite la production normale d’ATP dans la mitochondrie pour générer directement de la chaleur. Ce processus, appelé thermogénèse adaptative, permet de brûler des calories en dissipant l’énergie sous forme de chaleur, notamment en réponse au froid.
Chez l’humain, le tissu adipeux brun est très présent chez le nouveau-né (notamment entre les omoplates, autour du cou et des gros vaisseaux) afin de maintenir la température du corps. On a longtemps cru qu’il disparaissait presque totalement à l’âge adulte. Cependant, en 2009, plusieurs recherches s’appuyant sur la tomographie par émission de positons (PET Scan) ont démontré la présence de graisse brune active chez certains adultes, localisée principalement dans la région cervicale, les épaules et le long de la colonne vertébrale. Chez un adulte mince exposé au froid, ces dépôts de graisse brune captent du glucose et brûlent des acides gras pour produire de la chaleur, contribuant ainsi à la dépense énergétique. En revanche, la quantité de tissu adipeux brun chez l’adulte est hautement variable et tend à diminuer avec l’âge et avec l’excès de poids (les personnes obèses ou âgées en possèdent moins ou celui-ci reste inactif).
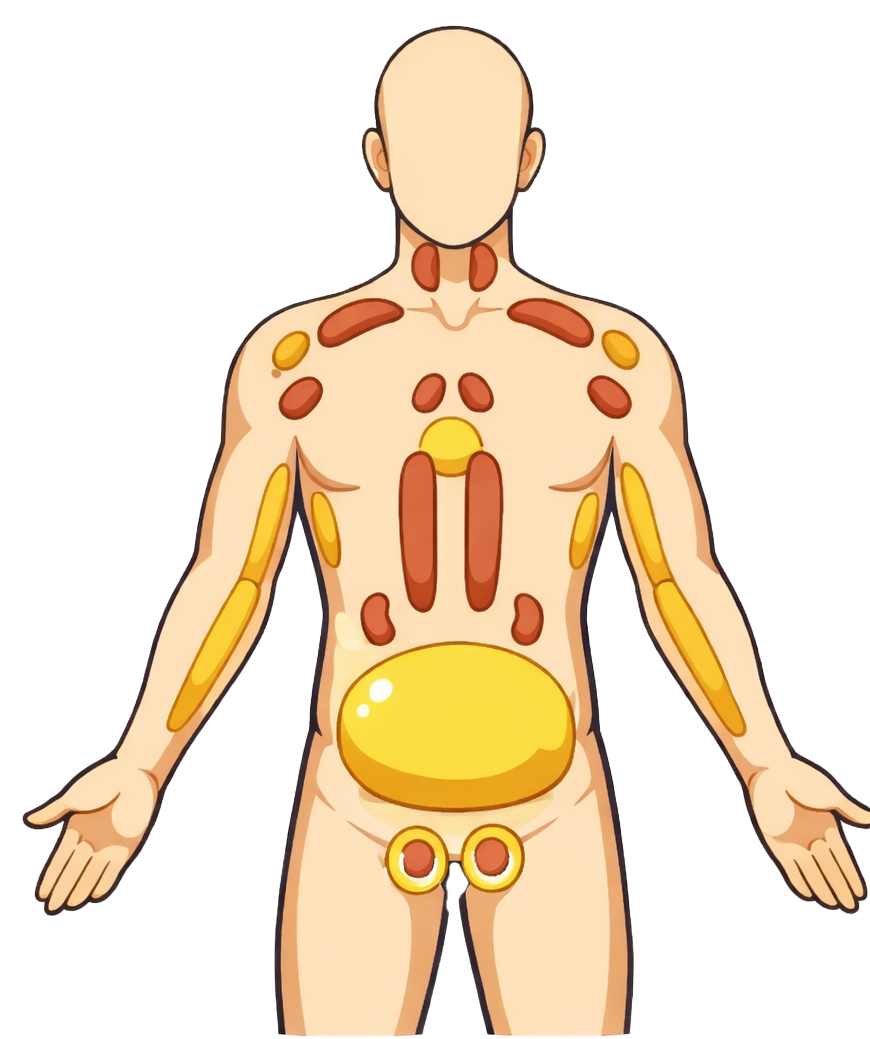
Le rôle physiologique principal du tissu adipeux brun est de maintenir la chaleur corporelle en conditions de froid. Il s’active sous le contrôle du système nerveux sympathique (catécholamines). Outre la thermogénèse, le TABr a également des fonctions endocrines émergentes : il sécrète des peptides et des lipides bioactifs (parfois appelés “batokines”) qui pourraient influencer le métabolisme global, bien que ces aspects soient encore à l’étude. Globalement, on peut voir la graisse brune comme un “radiateur” biologique, convertissant l’énergie en chaleur, à l’opposé de la graisse blanche qui agit plutôt comme un “réservoir” d’énergie. Cette opposition fonctionnelle en fait une cible de recherche attrayante pour lutter contre l’obésité, en cherchant à stimuler la dépense énergétique via le tissu brun. Toutefois, chez l’humain adulte, la masse de ce tissu adipeux brun est faible, et son impact métabolique global reste limité comparé à la graisse blanche.
Tissu adipeux beige
Entre le blanc et le brun, il existe une troisième catégorie d’adipocytes : les adipocytes beiges (parfois appelés adipocytes brite pour brown in white). Il ne s’agit pas d’un tissu adipeux distinct anatomiquement, mais plutôt de cellules brunes dispersées au sein du tissu adipeux blanc. En effet, dans certaines conditions, des adipocytes à mi-chemin entre le blanc et le brun apparaissent dans les dépôts de graisse blanche sous-cutanée. Ces adipocytes beiges présentent des caractéristiques intermédiaires : ils possèdent plusieurs gouttelettes lipidiques et des mitochondries avec de la thermogénine (comme les bruns), mais coexistent à côté d’adipocytes blancs uniloculaires classiques dans le même tissu.
Le phénomène d’apparition de ces adipocytes bruns induits au sein de la graisse blanche est appelé browning (littéralement brunissement du tissu adipeux blanc) ou beiging. Des stimuli externes comme l’exposition prolongée au froid ou la stimulation β-adrénergique (catécholamines) peuvent déclencher ce browning : le tissu adipeux blanc développe alors une fraction de cellules capables de thermogénèse, augmentant la dépense énergétique. Par exemple, des études montrent que quelques semaines d’exposition modérée au froid chez l’homme peuvent augmenter la masse et l’activité du tissu adipeux brun/beige, amélioration qui régresse dès le retour à un environnement chaud. De même, certains facteurs hormonaux liés à l’exercice physique ou à l’alimentation pourraient induire un browning. Dans ce cadre, l’irisine, une myokine libérée par le muscle pendant l’exercice, est notamment beaucoup étudiée comme possible déclencheur du browning, bien que les résultats soient encore débattus.
Les adipocytes beiges expriment UCP1 et peuvent, comme les adipocytes bruns, brûler des graisses pour produire de la chaleur. Toutefois, ils diffèrent des adipocytes bruns classiques sur le plan développemental et moléculaire. Alors que la graisse brune des nouveau-nés dérive d’une lignée de précurseurs commune aux cellules musculaires, les adipocytes beiges proviendraient plutôt de précurseurs présents dans le tissu blanc, capables de se différencier en adipocytes de type brun sous stimulation. Certains adipocytes blancs matures pourraient même se convertir en adipocytes beiges via un processus de transdifférenciation, en changeant de phénotype. Ce caractère est réversible : si le stimulus disparaît (par exemple, en repassant à une température chaude), les adipocytes beiges peuvent soit revenir à un phénotype blanc (perdant leurs mitochondries en excès et leur UCP1), soit disparaître par apoptose. Cette flexibilité illustre bien la plasticité cellulaire du tissu adipeux.
Le tissu adipeux beige intéresse beaucoup la recherche, car augmenter la proportion de “bonnes” graisses brunes/beiges au détriment de la graisse blanche pourrait théoriquement aider à brûler l’excès d’énergie chez les personnes en surpoids. Des études chez la souris ont montré que l’activation du browning améliore le métabolisme glucidique et la sensibilité à l’insuline. Néanmoins, chez l’humain, on ne sait pas encore induire un browning massif et soutenu de manière sûre et efficace. Le potentiel thérapeutique du tissu beige reste donc à confirmer, mais il constitue un bel exemple de la capacité du tissu adipeux à remodeler son phénotype fonctionnel en fonction des besoins de l’organisme.
| Comparaison des principaux types d’adipocytes chez l’humain. | |||
|---|---|---|---|
| Caractéristique | Adipocyte Blanc | Adipocyte Brun | Adipocyte Beige |
| Morphologie cellulaire | Grande cellule uniloculaire (1 grosse gouttelette lipidique) | Cellule multiloculaire (multiples petites gouttelettes) | Multiloculaire (dans un tissu blanc) |
| Taille typique | 50–150 µm (variable selon l’état nutritionnel) | 20–50 µm (plus petit que blanc) | Intermédiaire (taille similaire aux bruns) |
| Nombre de mitochondries | Faible (mitochondries peu abondantes) | Très abondant (riche en mitochondries contenant UCP1) | Abondant (exprime UCP1 sous stimulation) |
| Fonction principale | Stockage de l’énergie (triglycérides) | Dépense d’énergie par thermogenèse (production de chaleur) | Thermogenèse induite (dépend d’une stimulation, ex. froid) |
| Localisation | Partout dans le corps (sous-cutané, viscéral, etc.) | Zones spécifiques (nourrisson : interscapulaire. Adulte : cou, médiastin…) | Intégré dans du tissu blanc (surtout sous-cutané) |
| Rôle endocrine | Oui – production de leptine, adiponectine, etc. (nombreuses adipokines) | Oui – production de facteurs (ex. FGF21) mais rôle endocrine moins connu | Oui – similaire au brun quand activé (sécrétion de certaines adipokines) |
| Activation | Stimuli énergétiques (excès de calories → stockage, déficit → lipolyse) | Froid, stimulation β-adrénergique (sympathique) | Froid, stimulation β-adrénergique, hormones, exercice |
| Impact métabolique | Réserve calorique essentielle mais excès → syndrome métabolique | Augmente la dépense énergétique (peut protéger contre l’obésité) | Augmente légèrement la dépense énergétique (si activé) |
En résumé, la graisse blanche est le principal compartiment adipeux chez l’adulte, dédié au stockage d’énergie et à la signalisation hormonale. La graisse brune, plus abondante chez le bébé, permet de dépenser de l’énergie pour produire de la chaleur. Quant aux adipocytes beiges, ils représentent un potentiel adaptatif du tissu adipeux blanc, lui conférant la capacité de brûler des calories sous certaines conditions. La coexistence de ces types cellulaires souligne que le tissu adipeux est un organe plurifonctionnel et adaptable, bien loin de la vision monolithique que l’on en avait par le passé.
Distribution anatomique et diversité fonctionnelle des dépôts adipeux
Au-delà des différences de types cellulaires, la localisation anatomique des tissus adipeux joue un rôle déterminant dans leurs fonctions et leur impact sur la santé. Le corps humain possède de nombreux dépôts adipeux distincts, répartis de la tête aux pieds, qui se distinguent par leur anatomie, leur vascularisation, leur innervation et leurs interactions avec les organes voisins. Cette section explore la diversité anatomique du tissu adipeux et les conséquences fonctionnelles de la répartition des graisses.
Graisse sous-cutanée vs graisse viscérale
La distinction la plus classique en médecine et en sciences du sport oppose la graisse sous-cutanée (située sous la peau) à la graisse viscérale (accumulée à l’intérieur de la cavité abdominale, autour des organes). Il s’agit dans les deux cas de tissu adipeux blanc, mais leur comportement et leurs effets métaboliques divergent nettement.
Il est important de noter que la distinction sous-cutané/viscéral ne recouvre pas toutes les nuances. Par exemple, la graisse sous-cutanée abdominale profonde (située sous la couche musculaire) peut avoir un comportement métabolique intermédiaire. Néanmoins, cette opposition explique en grande partie pourquoi deux personnes de même IMC peuvent avoir des risques de maladie très différents : tout dépend si la graisse excédentaire est stockée de façon sous-cutanée “bénigne” ou viscérale “toxique”.
En pratique clinique et sportive, on évalue cette distribution en mesurant le tour de taille ou le rapport taille/hanche. Un tour de taille élevé signe une accumulation viscérale et un risque cardiométabolique accru, même chez des sujets non obèses en apparence (c’est le cas du profil TOFI, Thin Outside, Fat Inside, c’est-à-dire, maigre dehors, gras dedans). À l’inverse, un individu en surpoids à répartition plutôt gynoïde (hanches larges, taille modérée) pourrait présenter un risque moindre de diabète. Ainsi, la distribution anatomique du tissu adipeux est un facteur clé de son impact sur la santé.
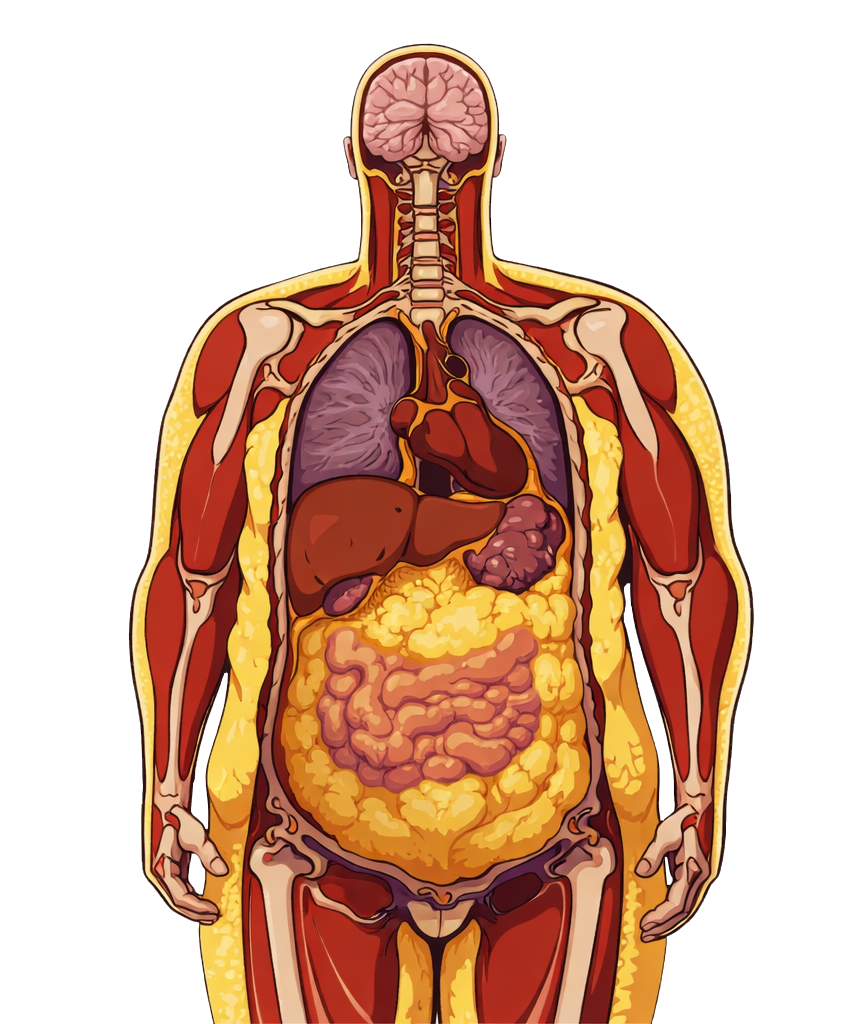
MUO (Metabolically Unhealthy Obesity) 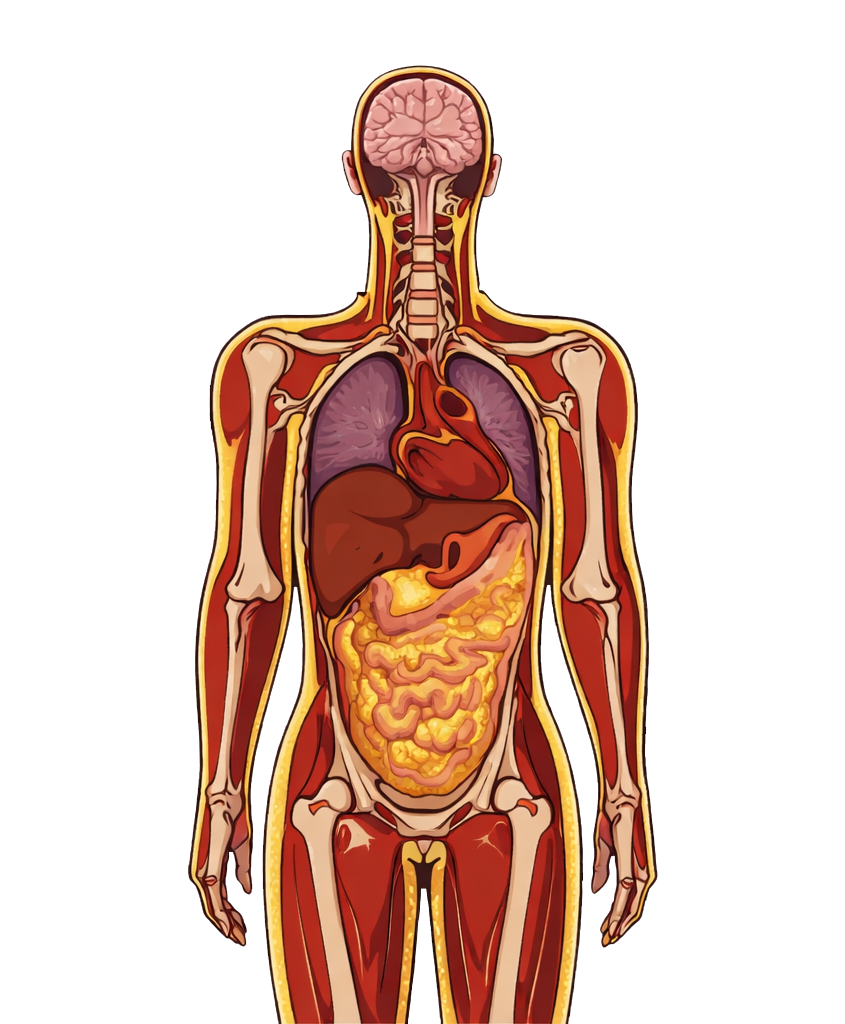
TOFI (Thin Outside, Fat Inside)
Pourquoi la graisse viscérale est-elle plus délétère que la graisse sous-cutanée ?
Plusieurs hypothèses non exclusives existent :
Dépôts adipeux spécifiques et rôles particuliers
Outre la graisse sous-cutanée et viscérale, le corps héberge des dépôts adipeux plus discrets mais aux fonctions souvent essentielles, parfois locales et non traditionnelles. En voici quelques exemples notables :
Cette liste n’est pas exhaustive : citons encore la graisse péritonéale (qui tapisse l’intérieur de la cavité abdominale), la graisse périrénale (autour des reins, jouant un rôle de maintien et de protection) ou la graisse orbitaire (derrière les globes oculaires, servant de support aux mouvements oculaires). Chacun de ces dépôts peut avoir des fonctions mécaniques et métaboliques spécifiques.
La diversité anatomique du tissu adipeux explique que l’on puisse parler de “tissus adipeux” au pluriel. Loin d’être homogène, le système adipeux du corps humain est une véritable mosaïque, chaque dépôt local pouvant s’adapter aux besoins de son environnement immédiat tout en contribuant à l’équilibre global. Certains dépôts exercent des fonctions vitales (thermogénèse, soutien énergétique local, régulation immunitaire de la peau, etc.), d’autres constituent des réserves mobilisables en cas de nécessité. Mais cette compartimentation a aussi un revers : selon où se stocke l’excès de graisse, les conséquences ne seront pas les mêmes. Par exemple, 1 kg de graisse en trop placé autour du foie ou du cœur aura bien plus de conséquences délétères que 1 kg réparti sous la peau des cuisses. Cette notion est essentielle pour évaluer le risque métabolique d’un individu et pour adapter les stratégies de gestion du poids. Elle explique aussi certaines contradictions apparentes dans les études : on peut avoir un IMC “normal” mais un excès de graisse viscérale caché et être à risque de diabète, ou inversement être obèse mais avec une bonne répartition et un tissu adipeux fonctionnel, et rester en meilleure santé métabolique (du moins temporairement).
En somme, l’emplacement compte autant que la quantité. Comprendre les particularités de chaque dépôt adipeux aide à interpréter les adaptations du corps (à l’exercice, au froid, à la suralimentation) et les mécanismes pathologiques de l’obésité. Voyons maintenant comment ces différents dépôts peuvent s’adapter (plasticité) ou au contraire dysfonctionner selon les sollicitations.
Plasticité et remodelage du tissu adipeux
Le tissu adipeux est souvent dépeint comme hautement plastique, c’est-à-dire capable de modifier sa structure et sa composition cellulaire en réponse aux changements de l’organisme ou de l’environnement. Cette plasticité s’exprime de multiples façons : expansion ou réduction de la masse graisseuse, remaniements cellulaires (hyperplasie, hypertrophie, différenciation), modifications de l’architecture vasculaire et de la matrice extracellulaire, changement du profil immunitaire du tissu, etc. Elle permet au tissu adipeux de remplir ses fonctions dans des conditions très variées (famine ou abondance, froid ou chaud, croissance, grossesse, etc.) mais connaît aussi des limites dont le franchissement mène au dysfonctionnement.
Browning / Beiging : l’émergence des adipocytes beiges
L’un des exemples les plus frappants de plasticité du tissu adipeux est le phénomène de browning du tissu adipeux blanc, déjà introduit plus haut. Pour rappel, il s’agit de la capacité du tissu blanc à acquérir des caractéristiques de tissu brun sous l’effet de certaines stimulations, via l’apparition d’adipocytes beiges thermogéniques. Ce processus illustre une plasticité phénotypique des adipocytes : une cellule de stockage peut, dans certaines limites, se reprogrammer en cellule de combustion.
Le browning est principalement induit par l’activation du système nerveux sympathique, typiquement lors d’une exposition prolongée au froid. Les nerfs sympathiques innervant le tissu adipeux libèrent de la noradrénaline, qui se fixe sur les récepteurs β-3 adrénergiques des adipocytes blancs. S’ensuit une cascade de signalisation (voie AMPc-PKA) aboutissant à l’expression de gènes caractéristiques des adipocytes bruns (comme UCP1) dans certaines cellules du dépôt blanc. Ces cellules augmentent leur nombre de mitochondries, fragmentent leur grande gouttelette lipidique en petites gouttelettes et commencent à oxyder des acides gras pour produire de la chaleur au lieu de les stocker. En parallèle, des précurseurs mésenchymateux présents dans le tissu adipeux peuvent être recrutés pour se différencier directement en adipocytes de type brun. Le résultat macroscopique, après quelques semaines de froid, est que le tissu adipeux blanc précédemment homogène présente une couleur plus brune et une activité métabolique accrue : c’est le tissu adipeux beige.
Le browning n’est cependant pas un état permanent : il dépend de la continuité de la stimulation. Si l’on supprime le stimulus (par exemple en réchauffant l’organisme), les adipocytes beiges perdent progressivement leur expression d’UCP1 et redeviennent “blancs” du point de vue fonctionnel. Cette réversibilité rapide a été montrée chez l’animal et dans les études chez l’homme exposé au froid : la biologie du tissu adipeux s’adapte en quelques jours ou semaines dans un sens comme dans l’autre. Cela suggère que les adipocytes beiges dérivés de blancs ne meurent pas forcément quand le froid cesse, mais peuvent redifférencier vers un phénotype stockage. Cette faculté est un sujet de recherche actif, car comprendre comment maintenir le browning pourrait être utile pour amplifier la dépense énergétique.
Hormis le froid, d’autres facteurs peuvent moduler le browning :
Le concept de browning a suscité beaucoup d’espoirs dans la lutte contre l’obésité, car il offre la perspective de dissiper l’énergie excédentaire en réorientant la fonction du tissu adipeux. Cependant, il faut garder à l’esprit que même activé, le tissu brun/beige chez l’adulte ne représente qu’une petite fraction de la masse grasse. La dépense calorique additionnelle réalisable par browning (quelques dizaines de kcal par jour dans les études réalistes) est insuffisante à elle seule pour compenser un régime hypercalorique ou induire une perte de poids majeure. De plus, augmenter la thermogenèse n’est pas sans risque (stress cardiovasculaire, ressentis de froid, etc.). Ainsi, le browning est un outil métabolique intéressant, surtout pour améliorer la glycémie et les lipides sanguins (en brûlant du glucose et des acides gras en excès), mais ce n’est pas une solution miracle à l’obésité. Son intérêt clinique pourrait résider en complément d’autres approches, par exemple pour aider des patients obèses à équilibrer leur diabète en augmentant leurs dépenses énergétiques sans effort physique intense.
En résumé, le browning illustre la plasticité fonctionnelle du tissu adipeux : en quelques jours, la même zone de graisse peut changer de fonction (passer du stockage au déstockage dissipatif) sans changer de place. Cela se fait via une reprogrammation de certains adipocytes et le recrutement de nouveaux adipocytes bruns. Ce processus, bénéfique dans certaines conditions (froid, exercice), témoigne de l’extraordinaire adaptabilité du tissu adipeux aux besoins énergétiques de l’organisme.
Hyperplasie vs hypertrophie : modes d’expansion du tissu adipeux
Lorsqu’un individu consomme plus de calories qu’il n’en dépense sur une période prolongée, l’excès énergétique doit être stocké quelque part. Le tissu adipeux blanc est le site principal de ce stockage. La prise de masse grasse fait intervenir deux mécanismes cellulaires distincts : l’hypertrophie et l’hyperplasie adipocytaire. La balance entre ces deux modes d’expansion conditionne en grande partie la santé du tissu adipeux et, par ricochet, la santé métabolique globale.

Hyperplasie 
Hypertrophie
Ces deux mécanismes peuvent bien sûr coexister, mais leur proportion relative diffère selon les individus, les dépôts adipeux et les circonstances. Cette proportion a d’importantes conséquences.
L’hypertrophie excessive des adipocytes est associée à un dysfonctionnement du tissu adipeux. L’hypertrophie s’accompagne d’une altération du profil de sécrétion adipocytaire. La taille adipocytaire est un facteur crucial : des adipocytes hypertrophiés ont un métabolisme et une sécrétion altérés, favorisant l’insulino-résistance*”. En clair, plus les adipocytes sont gros, plus ils dysfonctionnent**.
À l’inverse, l’hyperplasie adipocytaire est souvent considérée comme une expansion “saine” du tissu adipeux. En augmentant le nombre de cellules, on permet au tissu de stocker davantage de lipides sans que chaque adipocyte individuel n’atteigne une taille critique. Mieux vaut avoir 100 adipocytes remplis à 50% de leur capacité que 50 adipocytes remplis à 100%. De petits adipocytes, plus nombreux, maintiennent une meilleure sensibilité à l’insuline et un profil de sécrétion hormonale plus favorable (davantage d’adiponectine, moins de cytokines inflammatoires). Les études montrent que les individus obèses qui conservent des adipocytes de taille modérée, grâce à une hyperplasie active, ont un profil métabolique plus sain que ceux dont les adipocytes atteignent des volumes extrêmes.
Cela renvoie à la notion de “capacité d’expansion” du tissu adipeux : lorsque la capacité est bonne (beaucoup de nouveaux adipocytes peuvent être formés), le surplus énergétique est stocké de façon sûre dans le tissu adipeux, protégeant les autres organes. Mais si la capacité d’expansion est limitée (pas assez de nouvelles cellules), alors les adipocytes présents gonflent au-delà du raisonnable, puis le surplus “déborde” vers d’autres organes (foie, muscles). C’est le début des complications.
On pourrait alors penser que favoriser l’hyperplasie adipocytaire est toujours bénéfique. Ce n’est pas si simple. D’abord, tout le monde n’a pas la même réserve de préadipocytes ni la même propension génétique à l’hyperplasie. En effet, des déterminants génétiques influencent le plan de construction du tissu adipeux. Par exemple, certaines personnes ont dès la naissance plus d’adipocytes (les bébés ayant plus de cellules adipeuses auront moins besoin d’hypertrophie plus tard). Ensuite, une fois que le nombre d’adipocytes a augmenté (pendant l’enfance ou l’adolescence, périodes propices à l’hyperplasie), il a tendance à rester élevé même en cas d’amaigrissement. Les études isotopiques ont montré que le nombre d’adipocytes chez l’adulte est relativement fixe, on renouvellerait environ 10% de nos adipocytes chaque année, mais le nombre total change peu, sauf en cas de prise de poids massive. Cela signifie que l’hyperplasie adipocytaire, une fois survenue, laisse un héritage : si un individu a multiplié ses adipocytes pendant une phase d’obésité, il gardera ces adipocytes même après avoir maigri (mais ils seront vides). Or, un nombre élevé d’adipocytes vides peut faciliter une reprise de poids rapide, car ces cellules “sous-remplies” envoient potentiellement des signaux de besoin de remplissage (faible leptine par adipocyte, etc.). Ce phénomène est souvent avancé pour expliquer le rebond de poids fréquent après un régime restrictif. C’est en quelque sorte la contrepartie négative de l’hyperplasie.
Malgré cela, du point de vue purement métabolique, à poids égal, il vaut mieux avoir plus de petites cellules. Arner et collaborateurs (2010) ont par exemple montré que des obèses avec adipocytes hypertrophiés présentaient beaucoup plus d’insulino-résistance que des obèses de même IMC avec adipocytes plus petits et plus nombreux. De même, certains traitements antidiabétiques comme les thiazolidinediones (TZD) exploitent l’hyperplasie : ces agonistes de PPAR-γ augmentent la différenciation de nouveaux adipocytes, ce qui répartit mieux le stockage lipidique et améliore la sensibilité à l’insuline malgré une possible prise de poids supplémentaire.
Il faut noter que la capacité d’hyperplasie varie selon les dépôts adipeux. La graisse sous-cutanée a une bonne capacité à générer de nouveaux adipocytes, surtout dans la partie inférieure du corps. En revanche, la graisse viscérale a moins de préadipocytes disponibles ou activables, ce qui expliquerait pourquoi l’expansion viscérale s’accompagne très vite d’hypertrophie et de dysfonction. Ce constat est cohérent avec le fait qu’un excès calorique chronique se traduit d’abord par une extension du compartiment sous-cutané, puis quand celui-ci arrive à saturation, les graisses débordent vers le viscéral et les organes (c’est la théorie de du débordement lipidique). Ainsi, l’incapacité du tissu sous-cutané à recruter suffisamment d’adipocytes pour stocker l’excès de graisses serait un déclencheur du stockage viscéral et ectopique pathologique.
En résumé, l’hyperplasie adipocytaire serait un signe de plasticité positive, permettant un stockage extensible et métaboliquement neutre, tandis que l’hypertrophie excessive signerait un dépassement des capacités d’adaptation du tissu adipeux. Favoriser l’hyperplasie (dans certaines limites) pourrait être une approche pour maintenir une bonne santé métabolique malgré un gain de poids modéré, c’est ce qui est observé chez les obèses métaboliquement sains. À l’inverse, lorsque l’hypertrophie domine sans hyperplasie compensatoire, le tissu adipeux devient le moteur de troubles métaboliques. Les conséquences inflammatoires, endocrines et métaboliques de ce basculement seront abordées dans la section consacrée au dysfonctionnement adipocytaire.
Plasticité dans divers contextes physiologiques et pathologiques
Pour compléter ce panorama de la plasticité adipeuse, il est utile d’illustrer comment le tissu adipeux se comporte dans différentes situations de la vie courante ou de la pathologie. Nous avons déjà abondamment traité le cas de l’expansion dans l’obésité. Abordons brièvement d’autres contextes :
Jeûne prolongé et amaigrissement
Lors d’une restriction calorique importante, le tissu adipeux perd du volume par déstockage des triglycérides (lipolyse augmentée). Les adipocytes rétrécissent (parfois à des tailles inférieures à la normale). Mais le nombre d’adipocytes ne chute pas drastiquement : les cellules vides persistent, mais entrent en “repos”. Chez les personnes ayant subi un amaigrissement massif (régime sévère ou chirurgie bariatrique), on trouve un tissu adipeux composé de nombreux adipocytes petits, parfois atrophiques, avec une fibrose résiduelle. Le profil inflammatoire s’améliore nettement (moins de macrophages M1), mais la fibrose accumulée pendant l’obésité ne disparaît qu’en partie. Le tissu garde donc des séquelles structurales, ce qui pourrait limiter sa réexpansion ultérieure ou au contraire faciliter la régénération adipeuse (sujet non tranché). Le jeûne modifie aussi la composition cellulaire : par exemple, on observe une augmentation des adipocytes bruns/beiges (chez l’animal) malgré la perte de poids, peut-être pour compenser la baisse de thermogenèse due à la fonte du tissu adipeux blanc.
Exercice et entraînement
L’exercice physique régulier induit des adaptations systémiques, y compris dans le tissu adipeux. D’une part, l’exercice réduit la masse grasse en augmentant la dépense énergétique et l’oxydation des lipides. Il vise en priorité les dépôts viscéraux et ectopiques, ce sont généralement eux qui diminuent le plus vite. D’autre part, l’exercice améliore la vascularisation du tissu adipeux (via une meilleure perfusion), et il modifie le profil des cellules immunitaires dans le sens anti-inflammatoire. Des études ont montré qu’après plusieurs semaines d’entraînement, la sécrétion adipocytaire est modifiée : plus d’adiponectine, moins de TNF-α, par exemple. On a aussi suggéré que l’exercice pourrait stimuler le browning modérément, par l’irisine notamment, bien que l’effet soit léger chez l’homme. Ainsi, l’exercice confère au tissu adipeux un profil plus sain et plus plastique : les adipocytes deviennent plus petits, plus insulino-sensibles, la matrice est moins rigide, l’inflammation baisse. Cela participe à l’amélioration de la sensibilité à l’insuline et à la diminution du risque métabolique chez les personnes actives. Un autre aspect important est que l’exercice augmente la capacité des adipocytes à recycler les lipides rapidement entre stockage et utilisation. Chez les athlètes d’endurance, les adipocytes sont entraînés à libérer des acides gras pendant l’effort puis à se re-remplir ensuite sans dysfonctionnement, témoignant d’une grande flexibilité métabolique du tissu.
Grossesse et post-partum
La grossesse est un état hyperanabolique où l’organisme stocke de l’énergie pour le fœtus et l’allaitement futur. On observe chez la femme enceinte une augmentation programmée de la masse grasse, avec une hyperplasie adipocytaire marquée dans certaines régions (fesses, cuisses, bras). C’est un phénomène physiologique et hormonalement régulé. Le tissu adipeux se prépare ainsi à mobiliser des réserves pendant la fin de grossesse et l’allaitement. Ensuite, lors de l’allaitement, la prolactine et d’autres hormones induisent une mobilisation des graisses (lipolyse accrue) pour fournir des acides gras dans le lait, ce qui entraîne souvent une perte de poids progressive de la mère. Le remodelage du tissu adipeux pendant et après la grossesse est fascinant : non seulement les adipocytes changent de taille, mais comme vu plus tôt, dans la glande mammaire, ils peuvent se transdifférencier en cellules sécrétrices de lait. On a là un exemple extrême de plasticité, où l’adipocyte abdique temporairement sa fonction de stockage pour se muer en une autre cellule fonctionnelle. Après le sevrage, la plupart de ces cellules redeviendront des adipocytes. Cette cyclicité peut laisser des traces (par exemple, le nombre d’adipocytes mammaires peut augmenter après chaque cycle de lactation). D’un point de vue métabolique général, la grossesse induit une certaine insulinorésistance physiologique (pour épargner du glucose au fœtus), et le tissu adipeux y contribue en changeant ses sécrétions : plus de leptine, de résistine, etc. C’est normal et réversible après l’accouchement pour la plupart des femmes, preuve que ces altérations adipocytaires étaient bien programmées et non pathologiques (sauf si un diabète gestationnel survient, indiquant peut-être un dépassement des capacités d’adaptation du tissu).
Vieillissement
Avec l’âge, la distribution des graisses tend à se centraliser (plus de graisse viscérale, moins de sous-cutanée périphérique, en particulier chez les femmes post-ménopausées). Le tissu adipeux vieillissant perd en plasticité : il devient moins hyperplasique, plus fibreux, et récupère moins bien après un stress. On observe une baisse de la fraction de préadipocytes capables de se différencier. De plus, le tissu adipeux brun décline avec l’âge, ce qui réduit la thermogenèse adaptative (d’où une tendance à la prise de poids plus facile). Le microenvironnement immunitaire du tissu adipeux montre aussi une inflammation chronique de bas grade qui augmente (phénomène “inflammaging“). Tous ces changements contribuent à une plus grande incidence de résistance à l’insuline chez les personnes âgées pour un même IMC. En d’autres termes, le tissu adipeux d’une personne âgée est moins tolérant à un excès calorique : il se dérègle plus vite. Cela souligne l’importance de conserver une bonne condition physique qui, on l’a vu, aide à maintenir la plasticité adipocytaire via l’exercice et un régime adapté.
Stress chronique et cortisol
Le cortisol, hormone du stress, a un effet particulier sur la distribution des graisses : il favorise l’accumulation de graisse viscérale au détriment de la graisse sous-cutanée périphérique (c’est frappant dans le syndrome de Cushing où une obésité du tronc est très marquée, par exemple). Le cortisol inhibe aussi partiellement la formation de nouveaux adipocytes (il favorise plutôt le gonflement des adipocytes existants). Un stress chronique avec cortisol élevé pourrait donc réduire la plasticité hyperplasique et conduire à une hypertrophie viscérale.
Pathologies cachexiques (cancer, SIDA)
À l’opposé de l’obésité, certaines maladies provoquent une déplétion sévère du tissu adipeux, comme dans le cas de la cachexie (qui s’accompagne également d’une perte important de la masse musculaire). Dans le cas d’un cancer, des facteurs tumoraux dérèglent le métabolisme : ils provoquent une lipolyse massive et résistante à l’insuline, menant à une fonte rapide des graisses. Le tissu adipeux cachectique se distingue par une infiltration inflammatoire, une apoptose adipocytaire et une quasi absence d’adipocytes beiges/bruns (le corps, paradoxalement, arrête la thermogenèse adaptative pour économiser l’énergie, mais la dépense de base reste élevée du fait de la tumeur). C’est un domaine où les chercheurs essaient de comprendre comment la plasticité adipocytaire (ou son détournement par la tumeur) contribue à l’amaigrissement extrême.
En définitive, ces exemples multiples démontrent que le tissu adipeux est loin d’être statique. Il réagit finement à l’état nutritionnel, hormonal et environnemental. Cette plasticité adaptative est généralement bénéfique, permettant à l’organisme de stocker et mobiliser l’énergie de façon appropriée dans chaque situation. Cependant, il existe des points de rupture : lorsque les sollicitations dépassent la capacité d’adaptation du tissu, la plasticité s’atténue et le tissu bascule dans un état délétère (inflammation chronique, fibrose, mort cellulaire). L’équilibre entre remodelage réussi et remodelage raté détermine en grande partie si la prise de poids restera bénigne ou se traduira par une pathologie métabolique.
Dysfonctionnements du tissu adipeux dans l’obésité
L’obésité n’est pas simplement un excès de graisse corporelle, c’est aussi un état où la graisse se comporte différemment, de manière anormale du point de vue biologique. On parle parfois de maladie du tissu adipeux pour décrire le fait que, chez les personnes obèses (surtout avec obésité abdominale), le tissu adipeux présente des caractéristiques de dysfonctionnement. Et celui-ci se traduit par :
Ces anomalies au sein du tissu adipeux ont des conséquences systémiques lourdes : elles jouent un rôle central dans le développement du diabète de type 2, des maladies cardiovasculaires, de l’hypertension, de la NAFLD et d’autres complications associées à l’obésité. Dans cette section, nous allons analyser les différents aspects du tissu adipeux dysfonctionnel chez l’obèse et les mécanismes par lesquels ils contribuent aux maladies.
De l’expansion adaptative à l’expansion pathologique
Décortiquons les événements clés qui marquent le basculement vers une expansion pathologique du tissu adipeux. On peut considérer qu’il existe une sorte de point de rupture où le tissu adipeux, saturé, cesse d’être un allié du métabolisme pour en devenir un perturbateur. Plusieurs phénomènes intriqués contribuent à cette rupture : dépassement de la capacité de stockage sûre, hypoxie, insuffisance vasculaire, stress mécanique, altérations de la matrice extracellulaire et fibrose.
Capacité de stockage sûre dépassée : Ce concept signifie qu’un tissu adipeux sain peut emmagasiner un certain surplus de graisses alimentaires sans dommage ; au-delà d’un certain seuil, chaque calorie lipidique additionnelle à stocker deviendrait “dangereuse” car elle contribuerait à la dysfonction du tissu adipeux ou serait détournée vers d’autres organes. Ce seuil correspond à la fameuse limite d’expansion adipocytaire évoquée plus tôt. Quand cette limite est atteinte, on voit apparaître les complications.
Mais que se passe-t-il concrètement lorsque le tissu adipeux est plein ? Un des premiers problèmes est l’insuffisance de vascularisation. En phase d’expansion rapide, la croissance des adipocytes peut excéder la capacité du tissu à former de nouveaux vaisseaux sanguins pour les oxygéner correctement. On trouve alors dans les tissus adipeux hypertrophiques des zones d’hypoxie chronique. Les adipocytes en hypoxie déclenchent une réponse de stress via le facteur de transcription HIF-1α (Hypoxia Inducible Factor 1). Or, dans le tissu adipeux obèse, il a été montré que HIF-1α n’entraîne pas qu’une angiogenèse compensatoire : il active également tout un programme pro-inflammatoire et pro-fibrotique. Notamment, HIF-1 stimule l’expression de collagènes et d’inhibiteurs des enzymes qui dégradent le collagène, favorisant l’accumulation de matrice extracellulaire. Le résultat, c’est que l’hypoxie paradoxalement aboutit à une fibrose du tissu plutôt qu’à une correction efficace du déficit en vaisseaux. Cette fibrose crée un tissu cicatriciel rigide qui limite davantage l’expansion des adipocytes (c’est comme un corset fibreux qui étrangle les cellules en croissance).
C’est un cercle vicieux : l’hypoxie entraîne une fibrose qui provoque une réduction de plasticité, ce qui résulte en une hypoxie locale encore plus élevée.
Certains chercheurs suggèrent donc que l’hypertrophie adipocytaire ne serait pas problématique en soi, ce serait peut-être plutôt le fait que l’adipocyte ne puisse pas s’hypertrophier d’avantage. Il a été observé dans des modèles murins qu’en supprimant HIF-1α spécifiquement dans les adipocytes, on réduisait la fibrose du tissu adipeux obèse et on améliorait la sensibilité à l’insuline, soulignant l’importance de cette voie pathogène.
Parallèlement, l’insuffisance de vascularisation cause un problème de nutriments : les adipocytes en périphérie du lobule adipeux reçoivent en priorité l’insuline et le glucose, mais ceux au centre en manquent. Cela peut contribuer à l’hétérogénéité de taille et de fonction des adipocytes dans un même dépôt. Certains restent sensibles à l’insuline (périphérie), d’autres deviennent insulino-résistants et lipolytiques (centre hypoxique). Cette mosaïque dysfonctionnelle entretient des flux d’acides gras anormaux.
Stress mécanique de la matrice : À mesure que les adipocytes grossissent, ils exercent une pression mécanique sur les structures voisines et la matrice extracellulaire. La matrice (réseau de collagène et de protéoglycanes) doit s’étirer. Si l’adipocyte pousse plus fort que la matrice ne cède, il se produit une augmentation de la rigidité tissulaire et un feedback négatif sur les cellules. Les adipocytes et les préadipocytes possèdent des senseurs mécaniques (intégrines, jonctions focales) qui, lorsqu’ils détectent un substrat rigide, envoient un signal anti-différenciation. En conséquence, un stroma trop fibrosé et rigide peut bloquer l’adipogenèse (car les cellules sentent qu’il n’y a plus de place ou de flexibilité pour accueillir de nouvelles cellules). Cela fige la situation dans un mode hypertrophique. De plus, un stress mécanique direct sur un adipocyte (par exemple, deux adipocytes hypertrophiques se compressant l’un l’autre) peut déclencher la voie de signalisation de l’inflammasome (via des canaux ioniques sensibles à l’étirement), conduisant à la sécrétion d’IL-1β, une cytokine pro-inflammatoire. Ainsi, un tissu adipeux surchargé physiquement est un tissu qui envoie des signaux de détresse chimique.
La combinaison de l’hypoxie et du stress mécanique conduit à la mort cellulaire : Comme mentionné, ces facteurs combinés aboutissent souvent à la mort de certains adipocytes. L’hypoxie cause une nécrose du noyau d’un lobule adipeux, par manque d’ATP local, et la tension mécanique peut éclater la membrane cellulaire. La mort cellulaire (surtout nécrotique) est un événement déclencheur majeur pour l’inflammation : les contenus cellulaires s’échappent (acides gras, ADN, etc.) et agissent comme des signaux de danger pour les macrophages environnants. On passe alors d’une simple infiltration macrophagique modérée à une inflammation franche (voir partie suivante). D’un point de vue histologique, c’est l’apparition massive des couronnes de macrophages entourant les adipocytes morts qui signale ce basculement. C’est souvent à ce stade que l’on considère que le tissu adipeux est entré dans un état pathologique qui alimente les problèmes métaboliques plutôt que de les prévenir.
En résumé, tant que le tissu adipeux peut remodeler son infrastructure (vaisseaux, matrice) et recruter de nouvelles cellules, il absorbe l’excès d’énergie sans trop de heurts. Lorsqu’il ne le peut plus, l’expansion se fait par hypertrophie extrême, provoquant hypoxie, fibrose, stress cellulaire et mort adipocytaire. Ces anomalies locales (micro-hypoxie, fibrose segmentaire) sont caractéristiques du tissu adipeux obèse et pathologique, et rarement présentes dans un tissu adipeux sain même volumineux (par exemple, chez un sujet gagnant du poids modérément, sa graisse sous-cutanée s’agrandit mais reste bien oxygénée et peu fibrosée). De plus, l’échec du tissu adipeux à stocker conduit au stockage ectopique : quand la graisse ne peut plus entrer dans les adipocytes saturés, les lipides en surplus vont infiltrer d’autres organes (foie, muscle squelettique, cœur, pancréas…) où ils provoqueront des dysfonctions locales (d’où le terme lipotoxicité). Enfin, notez que la graisse viscérale a généralement une capacité d’hyperplasie plus faible que la graisse sous-cutanée, d’où le fait qu’elle devienne plus vite dysfonctionnelle en cas de surplus. Aussi, le seuil à partir duquel les problèmes surviennent diffère selon les individus.
Inflammation, immunité et sénescence : le basculement vers un tissu malade
Un trait marquant du tissu adipeux dysfonctionnel est la présence d’une inflammation chronique de bas grade en son sein. Cette inflammation adipocytaire locale, autrefois insoupçonnée, est désormais reconnue comme un élément central reliant l’obésité aux complications métaboliques. Dans cette section, nous examinons comment le système immunitaire du tissu adipeux bascule lors de l’expansion pathologique, avec l’afflux de macrophages pro-inflammatoires, l’implication d’autres cellules immunes, l’émergence de cellules sénescentes, et comment tout cela alimente le cercle vicieux de dysfonction.
Macrophages et inflammation adipocytaire :
Dans un tissu adipeux sain (par exemple chez un individu mince), les macrophages représentent environ 5 à 10% des cellules du tissu adipeux, et la plupart ont un phénotype anti-inflammatoire (qu’on appelle macrophages M2, impliqués dans l’homéostasie des tissus et la réparation). Ils nettoient les débris et aident à maintenir un environnement favorable. En revanche, dans le tissu adipeux obèse et hypertrophié, la proportion de macrophages peut grimper à 50% des cellules du stroma vasculaire ! La majorité de ces macrophages ont alors un phénotype pro-inflammatoire (dits de type M1) : ils expriment des marqueurs comme CD11c et sécrètent TNF-α, IL-6, IL-1β, MCP-1, etc. D’où viennent-ils ? L’hypertrophie adipocytaire entraîne la libération accrue de MCP-1 (CCL2), une chimiokine qui recrute les monocytes du sang vers le tissu adipeux. Une fois infiltrés, ces monocytes se différencient en macrophages M1. Par ailleurs, la mort adipocytaire fournit un puissant signal aux macrophages résidents pour proliférer localement (par des facteurs comme le GM-CSF). Il se forme alors des “couronnes” autour des adipocytes morts : des macrophages chargés de lipides qui les digèrent. Ce processus de phagocytose des restes lipidiques peut transformer les macrophages en cellules spumeuses similaires à celles qu’on voit dans les plaques d’athérosclérose, les poussant à produire plus de cytokines inflammatoires et d’enzymes (collagénases, etc.).
Les macrophages M1 dans la graisse obèse deviennent ainsi la principale source de cytokines inflammatoires locales, lesquelles diffusent aussi dans la circulation. Par exemple, l’IL-6 produite par la graisse contribue à élever la CRP (protéine C-réactive) hépatique, un marqueur d’inflammation systémique qu’on retrouve augmenté dans l’obésité. Le TNF-α, lui, interfère avec la signalisation de l’insuline (il phosphoryle IRS-1 sur des sérines inhibitrices), ce qui renforce l’insulino-résistance des adipocytes (et du muscle à travers la circulation).
Autres cellules immunitaires
Les macrophages ne sont pas seuls. Dès les premiers stades de la prise de poids, on voit apparaître dans le tissu adipeux des lymphocytes T qui modulent la réaction immunitaire. Des études chez la souris montrent qu’avant même l’afflux massif de macrophages, des lymphocytes T CD8+ infiltrent la graisse en réponse aux altérations, et qu’en les éliminant on peut retarder l’arrivée des macrophages. Ces lymphocytes T CD8+ pro-inflammatoires produisent eux aussi de l’IFN-γ et d’autres signaux qui activent les macrophages. Les lymphocytes T CD4+ (auxiliaires) peuvent basculer d’un profil Treg anti-inflammatoire à Th1 pro-inflammatoire dans l’obésité. On observe également une augmentation des cellules NK (Natural Killers) dans la graisse obèse, qui peuvent tuer des adipocytes stressés (via des ligands de NKG2D) ou stimuler les macrophages. Des mastocytes (cellules immunitaires de l’allergie) infiltrent aussi la graisse et libèrent des médiateurs qui aggravent l’inflammation. Même les neutrophiles font une apparition transitoire en début de régime hypercalorique, relâchant des enzymes et des radicaux libres. Ainsi, tout le système immunitaire inné et adaptatif converge vers la graisse en expansion pathologique, comme s’il s’agissait d’un tissu en souffrance qui nécessite une réaction de défense/réparation.
Malheureusement, cette réponse immunitaire chronique devient maladaptative. Au lieu de simplement réparer le tissu, elle le blesse davantage. L’inflammation chronique entretient la fibrose (via des facteurs comme le TGF-β libéré par les macrophages ou les mastocytes, stimulant les fibroblastes à produire du collagène). Elle génère des dommages oxydatifs : les macrophages activés produisent du NO et du superoxyde, qui peuvent se combiner en peroxynitrite, endommageant les cellules voisines. Ce stress oxydatif peut altérer encore plus la fonction des adipocytes restants (par exemple en oxydant les acides gras, ce qui peut perturber la signalisation de l’insuline).
Sénescence cellulaire
Un phénomène reliant l’inflammation et la perte de plasticité est la sénescence des cellules du tissu adipeux. La sénescence cellulaire est un état dans lequel une cellule arrête de se diviser et sécrète un panel de facteurs pro-inflammatoires et pro-dégradatifs (dont les cytokines pro-inflammatoires SASP). Dans le tissu adipeux vieillissant ou obèse, on trouve des adipocytes sénescents mais aussi des pré-adipocytes sénescents. Ces cellules sénescentes émettent des signaux (IL-6, IL-1β, MMPs…) qui amplifient le recrutement immunitaire et la dégradation tissulaire. Un préadipocyte sénescent ne peut plus se différencier en adipocyte, ce qui réduit la capacité hyperplasique. De plus, il peut entraver ses voisins en libérant des facteurs antagonistes (ex : activine A, qui inhibe l’adipogenèse). Ainsi, l’accumulation de cellules sénescentes dans la graisse obèse est un facteur aggravant de la dysfonction, verrouillant le tissu dans un état inflammatoire et rigide. Des travaux chez la souris ont montré que l’élimination pharmacologique des cellules sénescentes (via des sénolytiques) dans le tissu adipeux améliorait la glycémie et la fonction adipocytaire, soulignant leur rôle causal.
On peut désormais décrire le cercle vicieux complet se mettant en place dans un tissu adipeux dysfonctionnel :
L’hypertrophie adipocytaire cause hypoxie et mort cellulaire, cela attire et active des macrophages pro-inflammatoires qui libèrent TNF-α, IL-1β, etc. et qui aggravent l’insulino-résistance des adipocytes voisins et inhibent l’adipogenèse. Le tissu stocke de plus en plus mal le gras et grossit de manière désordonnée et plus d’adipocytes meurent. Les cytokines entretiennent la fibrose, or la fibrose et l’inflammation chroniques empêchent tout retour en arrière et endommagent encore plus la capacité de stockage entraînant par conséquent, plus de graisses circulantes, etc.
Ce cercle vicieux adipocytaire nourrit en parallèle un cercle vicieux systémique : l’inflammation adipocytaire conduit à une inflammation systémique modérée (hausse de CRP, cytokines circulantes) qui cause une résistance à l’insuline hépatique et musculaire, laquelle entraîne hyperglycémie et hyperinsulinémie, lesquelles stimulent encore la lipogenèse hépatique et la différenciation macrophagique… On voit comment tout s’auto-entretient, dessinant le tableau du syndrome métabolique complet.
Il est important de noter que cette inflammation est généralement silencieuse cliniquement (aucune douleur, pas de fièvre), mais elle est mesurable biologiquement (par des marqueurs comme la CRP ou l’IL-6 plasmatique). Elle n’est pas non plus aussi intense qu’une inflammation aiguë immunitaire, mais cette inflammation de bas grade constant suffit à perturber les organes cibles sur la durée.
Les conséquences directes pour le tissu adipeux lui-même sont une perte de fonction endocrine normale. Réduire cette inflammation est un objectif thérapeutique envisageable. Des études pilotes ont testé des anti-inflammatoires (comme la salicylate, un anti-inflammatoire faible, ou des antagonistes d’IL-1) chez des patients obèses diabétiques, montrant une amélioration modeste de la glycémie, confirmant que cibler l’inflammation adipocytaire peut aider. Cependant, éliminer entièrement l’inflammation n’est pas simple, car c’est une réponse intégrée de l’organisme face à l’excès nutritif. L’idéal est d’agir en amont en évitant que la taille des adipocytes ne déclenche cela, via des mesures d’hygiène alimentaire et physique précoces.
En conclusion, le basculement d’un tissu adipeux en tissu malade se caractérise par l’installation d’une inflammation chronique orchestrée par les macrophages et d’autres cellules immunes, ainsi que par l’apparition de cellules adipocytaires et progénitrices sénescentes. Cette inflammation entraîne une cascade de perturbations locales (fibrose, mort cellulaire continue) qui empêchent le tissu de remplir son rôle, et engendrent en parallèle des signaux à l’échelle du corps entier qui lèsent la sensibilité à l’insuline et la santé cardiovasculaire. Avec cet éclairage, nous pouvons aborder le dernier pan de la dysfonction adipocytaire : son rôle en tant qu’organe endocrine altéré, c’est-à-dire comment un tissu adipeux pathologique influence négativement le reste de l’organisme par ses sécrétions et son incapacité à réguler correctement le métabolisme général.
Organe endocrine altéré : le rôle des adipokines
Le terme adipokine désigne toute substance bioactive libérée par le tissu adipeux ayant un effet local ou systémique. Depuis la découverte de la leptine en 1994, des dizaines d’adipokines ont été identifiées, reflétant la polyvalence du tissu adipeux en tant que glande endocrine.
En plus d’être un site de stockage énergétique, le tissu adipeux agit comme un véritable organe endocrine. À ce titre, il sécrète une grande variété d’hormones, cytokines et médiateurs qui véhiculent des messages aux autres organes. Dans un état sain, il joue le rôle d’un chef d’orchestre métabolique raisonnable : il envoie des signaux hormonaux cohérents aux autres organes pour indiquer l’état des réserves énergétiques et maintenir l’équilibre du glucose, des lipides et de l’appétit. Mais lorsqu’il devient dysfonctionnel (hypertrophique, inflammatoire, fibrosé comme décrit précédemment), sa communication endocrine avec le reste du corps se dérègle dangereusement. Examinons dans cette partie les principaux changements dans le profil de sécrétion du tissu adipeux malade : baisse des adipokines protectrices, augmentation des facteurs délétères, et conséquences de ces altérations sur les organes cibles.
Leptine
C’est l’hormone emblématique du tissu adipeux, codée par le gène LEP (ou ob). La leptine est principalement secrétée par les adipocytes blancs en proportion de leurs réserves lipidiques. Plus on a de graisse, plus on produit de leptine. Son rôle principal est de signaler au cerveau (notamment à l’hypothalamus) l’état des réserves énergétiques. Une leptinémie élevée indique un stock de graisse abondant et induit au niveau central une diminution de l’appétit et une augmentation de la dépense énergétique (c’est un signal de satiété à long terme). Inversement, quand la masse grasse diminue, la leptine baisse, ce qui stimule la faim et réduit la dépense (mécanisme économiseur d’énergie). La leptine relie donc tissu adipeux et comportement alimentaire dans une boucle homéostatique. Elle a aussi des effets sur d’autres organes : elle régule la fonction reproductrice (un certain seuil de leptine est requis pour l’ovulation et la puberté, expliquant l’aménorrhée des femmes trop maigres), elle module l’immunité (c’est une cytokine de la famille IL-6, favorisant la réponse inflammatoire), et intervient dans la régulation de la pression artérielle (via le système sympathique).
Dans l’obésité commune, on observe une hyperleptinémie (excès de leptine) mais paradoxalement associée à un appétit conservé : c’est le phénomène de résistance à la leptine. Le cerveau des personnes obèses ne perçoit plus correctement le signal anorexigène de la leptine, possiblement à cause d’altérations des récepteurs ou du transport de la leptine vers l’hypothalamus. Conséquence : malgré des réserves pleines, l’appétit n’est pas correctement freiné. Ce concept de résistance leptinique rappelle celui de résistance à l’insuline, il s’agit d’un engrenage pathologique important de l’obésité. Par contraste, de rares individus ayant une mutation entraînant l’absence de leptine sont dans un état d’hyperphagie extrême et d’obésité morbide dès l’enfance, traitable par l’administration de leptine recombinante (un succès de la médecine moléculaire). Cela confirme à la fois le rôle crucial de la leptine dans la régulation pondérale et le fait que dans l’obésité commune, le problème n’est pas un manque de leptine mais une mauvaise réponse à celle-ci.
Adiponectine
C’est l’autre hormone majeure du tissu adipeux, mais avec un profil très différent. L’adiponectine est produite quasi exclusivement par les adipocytes blancs (et un peu par les beiges/bruns). Elle est particulièrement abondante dans le sang (c’est l’une des protéines les plus concentrées dans la circulation chez un sujet sain, autour de 5 à 10 µg/mL). L’adiponectine augmente la sensibilité à l’insuline dans le foie et les muscles : elle favorise l’oxydation des acides gras, la captation du glucose et diminue la production hépatique de glucose. Elle a aussi des effets anti-inflammatoires et anti-athérogènes (par exemple, elle inhibe l’adhésion des monocytes à l’endothélium vasculaire, modère l’activation macrophagique et stimule la production d’oxyde nitrique vasodilatateur). On parle souvent de l’adiponectine comme d’un facteur protecteur cardiovasculaire et métabolique. Fait notable, plus la masse grasse augmente, plus l’adiponectine diminue (c’est l’inverse de la leptine).
Les personnes obèses ont des taux bas d’adiponectine, ce qui contribue à l’insulino-résistance et à l’inflammation. Même au sein de la population, un taux bas d’adiponectine plasmatique est prédictif de diabète de type 2 et de maladie coronaire. Pourquoi l’adiponectine baisse-t-elle quand le tissu adipeux grossit ? On pense que l’hypertrophie adipocytaire et l’inflammation locale inhibent sa production. Le tissu adipeux viscéral en produit d’ailleurs beaucoup moins que le sous-cutané. Ainsi, l’adiponectine est un marqueur de santé du tissu adipeux : plus il est fonctionnel et équilibré, plus il en libère. Restaurer un niveau élevé d’adiponectine est un objectif thérapeutique intéressant. Certains médicaments comme les fibrates ou glitazones l’augmentent, tout comme la perte de poids ou l’exercice.
Résistine
Découverte chez la souris comme un lien entre obésité et résistance à l’insuline (d’où son nom), la résistine est une adipokine pro-inflammatoire. Chez les rongeurs, elle est produite par les adipocytes et élevée dans l’obésité, induisant du diabète. Chez l’humain, la situation est différente : la résistine est surtout sécrétée par les cellules immunitaires (macrophages) présentes dans le tissu adipeux, et non par les adipocytes eux-mêmes. Néanmoins, son taux sanguin est également plus haut en cas d’obésité et pourrait contribuer à l’insulino-résistance hépatique et à l’inflammation systémique. On la considère comme un marqueur de l’inflammation adipocytaire. Son rôle exact chez l’homme est moins élucidé que chez la souris, mais des études l’associent à l’athérosclérose, par exemple.
IL-6, TNF-α **et autres cytokines
Ce sont classiquement des cytokines immunitaires, mais le tissu adipeux (via ses macrophages et aussi les adipocytes pour TNF) en produit des quantités non négligeables. Dans l’obésité, jusqu’à 30% de l’IL-6 circulante pourrait provenir du tissu adipeux. L’IL-6 a des effets complexes : aiguë, elle favorise la lipolyse et la dépense énergétique (exercice), chronique, elle cause de l’inflammation et la résistance à l’insuline hépatique. Le TNF-α, lui, fut le premier facteur suspecté dans l’insulino-résistance de l’obésité : il est surproduit dans la graisse obèse et bloque la voie de l’insuline dans les adipocytes et muscles en phosphorylant le récepteur et IRS-1. Des souris sans TNF résistent mieux au diabète induit par l’obésité. Chez l’homme, les essais d’anticorps anti-TNF n’ont pas amélioré le diabète, peut-être parce que l’inflammation adipocytaire emprunte des voies redondantes. Néanmoins, le TNF-α adipocytaire reste un facteur local important de dysfonction : il stimule la lipolyse (donnant trop d’acides gras libres), il inhibe l’adiponectine, et il recrute plus de macrophages (auto-entretien de l’inflammation). D’autres cytokines pro-inflammatoires (IL-1β, MCP-1, etc.) sont également secrétées par le tissu adipeux en détresse et renforcent le syndrome inflammatoire.
Autres adipokines et facteurs
La liste est longue, mais voici quelques-uns des plus notables :
Visfatine (NAMPT) : identifiée initialement dans le tissu viscéral (d’où son nom), elle a un rôle enzymatique dans la voie NAD et peut agir comme cytokine pro-insuline (mimant l’insuline sur certains récepteurs). Son importance reste débattue.
Omentine : adipokine plutôt anti-inflammatoire et insulino-sensibilisante, produite surtout par le tissu adipeux viscéral chez les personnes maigres mais qui baisse en cas d’obésité.
Apeline : peptide produit par les adipocytes (et d’autres tissus), qui améliore la sensibilité à l’insuline et augmente avec l’obésité, peut-être pour compenser.
FGF21 : facteur de croissance fibroblastique 21, hormone métabolique surtout du foie mais aussi du tissu adipeux brun. Le tissu adipeux brun sécrète FGF21 lors de la thermogenèse, lequel agit globalement pour augmenter la dépense énergétique et la sensibilité insulinique. Il est en essai comme médicament potentiel.
Angiotensinogène : produit par le tissu adipeux et converti en angiotensine. II agit localement et systémiquement, il peut contribuer à l’hypertension associée à l’obésité (via rétention de sel, vasoconstriction).
PAI-1 : l’inhibiteur de l’activateur du plasminogène-1, fortement produit par la graisse viscérale, ce qui promeut un état pro-thrombotique (risque de caillots augmenté) chez les obèses.
Adipsine (Facteur D du complément) : une protéine du complément produite par les adipocytes, impliquée dans l’immunité innée. Récemment, on a découvert qu’elle pouvait améliorer la sécrétion d’insuline par les cellules bêta pancréatiques en protégeant une hormone (GLP-1) de la dégradation. L’adipsine a tendance à baisser en cas d’obésité avancée, ce qui pourrait contribuer à l’épuisement des cellules bêta.
RBP4 (Retinol-binding protein 4) : protéine de transport du rétinol produite par les adipocytes, augmentée dans l’obésité et impliquée dans l’insulino-résistance périphérique en perturbant la signalisation insulinique des muscles.
Signaux lipidiques : le tissu adipeux libère aussi des acides gras spécifiques, des céramides, des endocannabinoïdes, etc., qui agissent comme signaux paracrines ou endocrines. Par exemple, un excès d’acides gras saturés en circulation (provenant du tissu adipeux) peut activer les récepteurs de type Toll dans le système immunitaire inné et provoquer une inflammation (d’où l’idée que les acides gras libres eux-mêmes sont des “lipokines” pro-inflammatoires). À l’inverse, certains lipides produits par le tissu adipeux brun (acides gras oxydés) pourraient agir sur le foie ou le cœur de manière bénéfique.
Exosomes et microARN : le tissu adipeux libère dans la circulation des vésicules (exosomes) contenant des ARN non-codants (microARN) et des protéines qui peuvent influencer à distance l’expression génique dans d’autres organes. Par exemple, on a identifié des microARN adipocytaires qui modulent la sensibilité à l’insuline des muscles. Ce mode de communication inter-cellulaire est un domaine émergent.
SFRP5 : C’est une adipokine anti-inflammatoire (inhibiteur de la voie Wnt) qui est produite par le tissu adipeux sain. En obésité, son expression diminue, levant un frein sur l’inflammation dans les macrophages (par Wnt5a).
Cette liste démontre que le tissu adipeux est l’une des glandes endocrines les plus polyglottes du corps humain. Il parle le langage des hormones métaboliques, des cytokines immunitaires, des facteurs de croissance, des lipides bioactifs, etc. En temps normal, cette symphonie d’adipokines contribue à l’équilibre : la leptine assure que le poids reste stable, l’adiponectine protège les artères et la glycémie, les petites cytokines entretiennent une vigilance immunitaire locale, etc. En cas d’obésité, la partition se désaccorde : la leptine crie mais n’est plus entendue, l’adiponectine se tait, et les trompettes de l’inflammation dominent l’orchestre.
En plus de ces adipokines protéiques, un tissu adipeux dysfonctionnel libère en excès des acides gras libres (AGL) dans la circulation, surtout en phase postprandiale ou nocturne, du fait de son insulinorésistance. Ces AGL élevés ont leurs propres effets endocrines délétères : ils induisent une résistance à l’insuline hépatique, diminuent la captation de glucose musculaire (compétition énergétique), et stimulent la production exagérée d’insuline par le pancréas (car le pancréas sent plus d’AGL comme substrat et sécrète davantage d’insuline pour les métaboliser, c’est le concept de “glucolipotoxicité”). Ces AGL peuvent aussi s’accumuler dans le cœur provoquant des troubles cardiaques (lipotoxicité cardiaque). Donc le tissu adipeux malade agit aussi via cet envoi massif de lipides vers le sang, imposant aux autres organes une charge qu’ils ne devraient pas avoir.
Communication avec les organes cibles (cerveau, muscle, foie, etc.)
Les adipokines exercent leurs effets sur pratiquement tous les organes. Le tissu adipeux est un acteur central d’un réseau de communication complexe appelé parfois “adipoaxis“, en parallèle des axes classiques endocriniens. Résumons les principales interactions organe-par-organe :
Cerveau (hypothalamus)
Le duo leptine/insuline informe le cerveau des réserves énergétiques. Lorsque les adipocytes sont remplis, la leptine (couplée à l’insuline pancréatique post-prandiale) active dans l’hypothalamus des neurones anorexigènes (POMC/CART) et inhibe des neurones orexigènes (NPY/AgRP). Cela conduit à une diminution de la prise alimentaire et une augmentation de la dépense (via activation du système sympathique). Le cerveau reçoit aussi d’autres signaux adipocytaires : par ex, les acides gras libres circulants (libérés en lipolyse) peuvent traverser la barrière hémato-encéphalique et moduler la sensibilité de certains neurones à l’insuline ou la leptine.
Dans l’obésité, la résistance à la leptine dans l’hypothalamus conduit à une sorte de “surdose” de signal orexigène (AgRP élevé, etc.) malgré la pléthore calorique. Le cerveau se comporte comme s’il fallait stocker plus. C’est une altération majeure de la communication entre le tissu adipeux et le cerveau. À l’inverse, dans l’anorexie ou après un régime sévère, la leptine basse déclenche des réponses hyperphagiques et hypométaboliques très puissantes qui compliquent la stabilisation du poids perdu (le corps “défend” ses réserves). Cela illustre comment le tissu adipeux, via la leptine, fait partie intégrante du système de contrôle de l’appétit.
Muscles
Les muscles utilisent les acides gras comme carburant, fournis en partie par le tissu adipeux. Une adipose saine, sensible à l’insuline, libère les acides gras au bon moment (effort, jeûne) et les stocke après les repas, évitant ainsi aux muscles d’être submergés de lipides quand ils n’en ont pas besoin. Par ailleurs, l’adiponectine augmente l’oxydation des acides gras dans le muscle et la captation de glucose, elle agit via ses récepteurs (AdipoR1) pour activer des kinases (AMPK) stimulant le métabolisme musculaire. Donc, plus d’adiponectine équivaut à des muscles qui brûlent mieux le gras et le glucose.
En cas d’obésité (adiponectine basse, acides gras libres élevés), les muscles accumulent des lipides toxiques (céramides, diacylglycérol) qui perturbent la signalisation de l’insuline (PKC activation, etc.) et causent une résistance à l’insuline musculaire. On voit ainsi comment un tissu adipeux dysfonctionnel induit une myopathie métabolique. À l’inverse, un muscle entraîné sécrète des myokines (IL-6 musculaire, irisine, myostatine, etc.) qui vont moduler le tissu adipeux en retour : l’IL-6 de l’exercice améliore la lipolyse et peut réduire localement l’inflammation du tissu adipeux, l’irisine favorise le browning, etc.
Foie
Le foie est intimement lié au tissu adipeux, notamment via la circulation portale (en référence à la veine porte) pour la graisse viscérale. Un flux élevé d’acides gras libres venant du tissu adipeux aboutit dans le foie et peut entraîner une stéatose hépatique non alcoolique (NAFLD), littéralement un stockage de graisse ectopique dans les hépatocytes, car ceux-ci reçoivent plus d’acides gras qu’ils n’en brûlent ou n’en exportent. Par ailleurs, les adipokines influencent l’homéostasie hépatique : l’adiponectine a un effet anti-stéatose et anti-inflammatoire sur le foie (elle active AMPK dans le foie, réduisant la production de glucose et de lipides, et atténue l’inflammation hépatique).
En obésité, la baisse d’adiponectine et l’afflux de résistine, TNF, IL-6, aggravent l’insulinorésistance hépatique : le foie devient moins sensible à l’insuline, continue de produire trop de glucose et de VLDL, tout en stockant plus de graisse. Le résultat est le fameux foie gras métabolique qui accompagne souvent l’obésité viscérale. L’axe tissu adipeux–foie est donc central dans le syndrome métabolique. Certains parlent de l’adiponectine comme d’une “insuline hépatique” tant son action y est bénéfique, et de la résistine/TNF comme de “contre-insuline hépatiques”. D’un autre côté, le foie influence le tissu adipeux via la production de facteurs (par ex. IGF-1, hormones sexuelles liées au foie, etc.), mais c’est moins direct.
Tissu adipeux lui-même (auto/paracrine)
Il ne faut pas oublier que la plupart de ces adipokines agissent aussi sur le tissu adipeux lui-même. Par exemple, la leptine a des effets autocrines sur l’adipocyte (elle peut limiter la synthèse lipidique), l’adiponectine pourrait agir localement pour réguler la différenciation préadipocytaire, le TNF-α local inhibe directement l’accumulation de triglycérides dans l’adipocyte (il pousse à la lipolyse). Donc le profil de sécrétion du tissu adipeux module sa propre plasticité : trop de TNF et pas assez d’adiponectine, et les préadipocytes ne se différencient plus bien (inhibant l’hyperplasie); trop de leptine localement pourrait limiter le stockage. Ce système local est complexe et encore en étude.
Pancréas (cellules β)
Le tissu adipeux envoie des signaux au pancréas. Par exemple, la leptine peut agir sur les îlots pancréatiques en inhibant quelque peu la sécrétion d’insuline (effet anti-obésité potentiel, car moins d’insuline équivaut à moins de stockage de gras). Dans l’obésité, la leptine élevée maintient une certaine pression pour limiter l’hyperinsulinisme, mais la résistance leptinique centrale peut contrecarrer cela. L’adiponectine, via ses effets sur la sensibilité à l’insuline, allège la charge sur les cellules β, et possiblement a un effet direct cytoprotecteur sur ces cellules.
Au contraire, des acides gras en excès provenant du tissu adipeux causent une “lipotoxicité” des cellules β, réduisant leur fonction et conduisant à l’apoptose. On suspecte aussi qu’une adipokine comme adipsine (mentionnée plus haut) aiderait les cellules β en augmentant la durée d’action du GLP-1, ce qui boosterait la sécrétion d’insuline de manière glucose-dépendante. Dans l’obésité avancée, la conjonction de résistance insulinique (imposant une suractivité des cellules β) et de lipotoxicité (affaiblissant les cellules β) conduit souvent à un épuisement pancréatique, donc au diabète de type 2. Le tissu adipeux a une responsabilité double : c’est à cause de lui que le corps a besoin de beaucoup d’insuline (résistance périphérique), et c’est à cause de lui aussi que les cellules β flanchent (agression par les lipides et cytokines). Ainsi, un tissu adipeux dysfonctionnel, par la boucle hormonale, mène le pancréas à la faillite.
Reins
La concentration élevée de leptine dans l’obésité stimule le système sympathique rénal et pourrait contribuer à la réabsorption accrue de sodium, donc à l’hypertension. De plus, le tissu adipeux viscéral et périrénal produit de l’angiotensine II localement, renforçant la vasoconstriction. L’hyperinsulinisme (secondaire au tissu adipeux résistant) stimule aussi la réabsorption de sel par le rein. Tout cela fait du tissu adipeux un complice dans l’hypertension liée à l’obésité. Par ailleurs, l’obésité s’accompagne d’une graisse périnéphrique et périvasculaire rénale en expansion, qui pourrait favoriser une inflammation locale et de la fibrose rénale via les adipokines. On voit alors émerger la notion de lipotoxicité rénale.
Cœur et vaisseaux
L’adiponectine a des effets protecteurs sur le myocarde (anti-apoptotique, et prévient l’hypertrophie cardiaque induite par la pression). Une baisse d’adiponectine chez l’obèse peut ainsi favoriser la cardiomyopathie diabétique. La leptine, en excès, a des effets pro-hypertrophiques sur le cœur et peut favoriser des arythmies via le sympathique. Au niveau vasculaire, un profil adipokinique malsain (beaucoup de TNF, IL-6, angiotensine, peu d’adiponectine) cause une dysfonction endothéliale, une inflammation de la paroi vasculaire et la progression de l’athérosclérose. On attribue notamment au tissu adipeux viscéral un rôle dans le développement de l’athérosclérose coronarienne (via l’IL-6 élevée qui augmente la CRP et l’angiotensine II qui favorise l’hypertension). Ainsi, les maladies cardiovasculaires liées à l’obésité sont en bonne partie médiées par les adipokines. On peut dire que l’athérosclérose est une conséquence distante de l’inflammation du tissu adipeux.
Système immunitaire
Le tissu adipeux, via leptine et adipokines, influence le fonctionnement immunitaire global. La leptine, par exemple, stimule le système immunitaire inné (activation des macrophages, neutrophiles) et oriente l’immunité adaptative vers une réponse Th1 pro-inflammatoire plutôt que Th2. Les personnes très minces ou en dénutrition (faible leptine) ont souvent une immunité affaiblie, tandis que les obèses ont un système immunitaire suractivé mais de manière aberrante (inflammation chronique mais moindre réponse aux infections spécifiques). Cela a été observé avec la COVID-19 : l’obésité était un facteur de risque de forme grave, possiblement en raison d’un terrain inflammatoire de bas grade amplifiant la tempête cytokinique. L’adiponectine, de son côté, tempère certaines fonctions macrophagiques et peut augmenter les cellules anti-inflammatoires. Le tissu adipeux sécrète aussi des composants du système du complément (adipsine etc.), participant à l’immunité humorale. On commence à comprendre que le tissu adipeux pourrait être un organe immunitaire en soi, modulant l’équilibre entre tolérance et inflammation dans l’organisme.
On pourrait continuer avec d’autres organes (os, peau, glandes endocrines, etc.)… Par exemple, la leptine influence l’axe gonadotrope (des taux trop bas inhibent la fertilité, des taux très hauts pourraient aussi perturber la spermatogenèse ou la fonction ovarienne), la graisse dermique comme mentionné aide la peau à se défendre, etc. Mais retenons l’essentiel : le tissu adipeux dialogue avec presque tous les systèmes de l’organisme. Il envoie des signaux sur l’état énergétique, sur l’inflammation, sur la croissance, sur la vascularisation, et reçoit en retour des signaux hormonaux (insuline, hormones sexuelles, cortisol, adrénaline…) qui modulent son activité. Cette intégration multi-systèmes fait du tissu adipeux un organe clé pour le maintien de l’équilibre interne (homéostasie).
Ainsi, un tissu adipeux dysfonctionnel peut être qualifié d’organe endocrine pathogène : au lieu de remplir son rôle régulateur, il envoie des signaux aberrants à l’organisme qui induisent ou exacerbent les maladies métaboliques. Dans la perspective de traitements, une stratégie vise à restaurer un profil adipokine plus sain (par exemple, on a cherché des moyens d’augmenter l’adiponectine, ou des analogues de leptine pour vaincre la résistance, etc., avec succès limité jusqu’ici). Cependant, la normalisation durable du profil endocrinien adipocytaire passe souvent par la réduction de la masse grasse et la restauration de la plasticité (via perte de poids ou interventions sur la qualité du tissu, voir la partie suivante).
Résumé
Devant cette cascade de conséquences, on pourrait dire que l’obésité est d’abord et avant tout une maladie du tissu adipeux. C’est le dysfonctionnement de ce dernier (plus que la surcharge pondérale en soi) qui déclenche les pathologies associées. D’ailleurs, des personnes peuvent être obèses sans avoir tant de problèmes métaboliques apparents, ce que l’on nomme l’obésité métaboliquement saine, ce sont souvent celles dont le tissu adipeux, bien qu’abondant, est resté relativement fonctionnel (moins graisse viscérale, adipocytes pas trop gros, peu de fibrose, bonne hyperplasie, adipokines pas trop déréglées). À l’opposé, des personnes de corpulence modérée peuvent avoir un tissu adipeux très dysfonctionnel (par ex. beaucoup de graisse viscérale, infiltration ectopique) et développer un diabète ou un infarctus. C’est pourquoi il faut insister sur le concept de qualité du tissu adipeux.
Aujourd’hui, certains chercheurs proposent que l’évaluation du risque chez un patient en surpoids ne devrait pas se limiter à son poids ou à l’IMC, mais chercher des marqueurs du fonctionnement adipocytaire : distribution des graisses (tour de taille, imagerie), dosage d’adipokines clés (adiponectine, leptine), indices de lipolyse excessive (acides gras libres élevés), etc. Par exemple, un faible ratio adiponectine/leptine dans le sang est associé à la résistance à l’insuline et pourrait refléter un tissu adipeux en souffrance.
En résumé, le tissu adipeux dysfonctionnel est le fil conducteur de la pathogénie de l’obésité. Il convertit un surplus énergétique chronique en une cascade de signaux pathogènes qui touchent presque tous les organes. La bonne nouvelle est que si l’on parvient à “resynchroniser” ce tissu, principalement par la perte de graisse, mais aussi par d’autres interventions, beaucoup de ces anomalies régressent. C’est le principe de base du traitement de l’obésité : améliorer la fonction adipeuse en diminuant la charge et en modifiant le mode de vie de sorte à rendre la graisse restante plus saine. Nous allons voir justement dans la section suivante quelles sont les implications cliniques de tout ceci et les stratégies thérapeutiques actuelles ou futures pour prendre en charge un tissu adipeux dysfonctionnel.
Implications cliniques et thérapeutiques
Les connaissances sur la biologie du tissu adipeux ont des retombées concrètes pour la prise en charge de l’obésité, du diabète et des maladies métaboliques. Comprendre qu’il s’agit d’une maladie du tissu adipeux oriente la stratégie thérapeutique : il ne suffit pas de réduire la masse grasse, il faut aussi tenter d’améliorer sa fonction. Dans cette section, nous discuterons de quelques implications pratiques : comment évaluer le tissu adipeux d’un patient (au-delà du poids), comment le style de vie peut influencer la santé du tissu adipeux, quels traitements ciblent directement ou indirectement le tissu adipeux, et quelles sont les limites et perspectives de ces approches.
Évaluation clinique du tissu adipeux : au-delà du poids
En pratique clinique (ou même en coaching sportif), l’IMC n’est qu’un point de départ. Deux personnes de même IMC peuvent avoir des profils adipocytaires très différents. Il est donc important d’évaluer la distribution des graisses et certains marqueurs biologiques pour affiner le tableau.
En somme, aucun test isolé n’est suffisant, mais un ensemble d’indices (ex : patient pas très lourd mais tour de taille élevé, adiponectine basse, triglycérides hauts, HDL bas, etc.) signera une atteinte du tissu adipeux viscéral.
Du point de vue du patient ou du sportif, l’évaluation doit faire prendre conscience que toute prise de poids n’est pas égale. Il vaut mieux du poids pris en muscle ou en graisse sous-cutanée périphérique que du poids pris en graisse abdominale. De même, en perte de poids, viser la réduction de la ceinture abdominale est prioritaire.
En clinique du sport, on peut rencontrer des athlètes avec un IMC normal mais un taux de graisse viscérale élevé (en particulier certains sports de force où on ne fait pas trop de cardio). Ces sujets peuvent bénéficier d’examens type DEXA ou IRM pour les alerter sur leur composition corporelle réelle.
En médecine, la compréhension fine de la distribution adipocytaire a amené la notion de phénotypes : obésité “métaboliquement saine” vs “métaboliquement malsaine”. On pourrait affiner encore en identifiant un “phénotype fibrose adipocytaire” ou “phénotype inflammatoire” via des biopsies de graisse. En pratique, on ne réalise pas de biopsie de graisse de routine, sauf pour la recherche ou suspicion de pathologie rare, mais peut-être un jour ?
Mode de vie, exercice et amélioration de la santé adipocytaire
Comme souvent, les interventions sur le mode de vie sont la pierre angulaire du traitement, et elles ont des effets profonds sur le tissu adipeux.
Pour les patients, il faut insister sur le fait que même sans perte de poids majeure, l’exercice améliore la composition corporelle et la santé métabolique. On voit ainsi des patients perdre peu de kilos mais beaucoup de centimètres de tour de taille grâce au sport : cela signifie que la graisse viscérale a fondu et que la masse maigre a augmenté, ce qui peut se compenser sur la balance mais faire une énorme différence sur la santé. Toute augmentation de l’activité physique (marche, sport, renforcement musculaire) est bénéfique pour “traiter” un tissu adipeux problématique.
En somme, le mode de vie peut transformer radicalement le comportement du tissu adipeux. L’alimentation équilibrée et l’exercice régulier transforment un tissu adipeux “malade” en un tissu plus “sain”, plus petit, plus insulino-sensible, moins inflammatoire. L’impact positif sur la santé vient largement de là. On pourrait presque dire que l’objectif d’une prise en charge diétético-physique est de restaurer la plasticité adipocytaire : rendre au tissu adipeux sa capacité à absorber l’énergie sans provoquer d’inflammation, et sa capacité à en libérer quand il faut.
Approches thérapeutiques ciblant le tissu adipeux
En plus des mesures d’hygiène de vie, il existe plusieurs approches médicales (pharmacologiques ou chirurgicales) qui visent soit à réduire la masse grasse, soit à modifier le fonctionnement du tissu adipeux. Présentons les principales :
Médicaments favorisant la perte de poids : La pharmacopée anti-obésité a longtemps été limitée, mais de récentes avancées ont transformé le paysage.
Les analogues du GLP-1 (liraglutide, sémaglutide, etc.) administrés en injection sont initialement des antidiabétiques qui se sont révélés très efficaces pour induire une perte de poids significative (–10 à –15% en moyenne). Ils agissent en diminuant fortement l’appétit et en retardant la vidange gastrique. Indirectement, en réduisant les apports, ils mettent le tissu adipeux en déficit, donc enclenchent sa déplétion. On a observé qu’au-delà de la perte de masse grasse, ces molécules améliorent la sensibilité à l’insuline et réduisent l’inflammation systémique, suggérant un effet bénéfique sur la fonction adipocytaire (peut-être via une baisse de leptine et une hausse relative d’adiponectine). Par exemple, un an de sémaglutide peut quasiment “guérir” un diabète de type 2 chez un patient obèse, ce qui signifie que son tissu adipeux a beaucoup maigri et retrouvé un équilibre hormonal convenable. Ces médicaments sont en train de révolutionner la prise en charge de l’obésité sévère, dans la mesure où ils offrent une perte de poids importante sans chirurgie, ce qui allège durablement la charge sur le tissu adipeux.
Les inhibiteurs de SGLT2 (gliflozines) sont aussi des antidiabétiques induisant une perte de poids modeste (–2 à –3%) en provoquant une perte de glucose dans les urines. Ils ne ciblent pas spécifiquement le tissu adipeux, mais en induisant un déficit calorique, ils forcent un peu la lipolyse. Ils peuvent réduire légèrement la graisse viscérale. Pas une panacée pour l’obésité, mais utiles chez le patient diabétique pour qui un peu de poids en moins aide.
Les agonistes des récepteurs β3 (comme le mirabégron, un médicament urologique) ont été testés pour activer la graisse brune. Une dose élevée de mirabégron peut augmenter la dépense énergétique de repos d’environ 100 kcal/jour via le tissu adipeux brun, ce qui n’est pas négligeable. Toutefois, ces doses élevées peuvent aussi provoquer tachycardie et hypertension (le mirabégron aux doses standard a moins cet effet). Ce n’est pas (encore) approuvé pour l’obésité, mais c’est une piste. D’autres substances comme l’éphédrine (stimulant adrénergique) ont été utilisées par le passé pour augmenter la thermogenèse, mais au prix d’effets cardio-vasculaires négatifs. La recherche pharmaceutique tente de trouver des molécules qui activent la graisse brune sans stimuler le cœur, ou qui induisent un browning sélectif.
Les thiazolidinediones (TZD), tels que la pioglitazone, méritent qu’on s’y attarde. Utilisés pour traiter le diabète de type 2, ils agissent en activant le facteur de transcription PPAR-γ qui est le “maître-régulateur” de l’adipogenèse. En conséquence, ces médicaments augmentent l’hyperplasie adipocytaire et le stockage lipidique dans le tissu adipeux sous-cutané. Cliniquement, les patients sous TZD prennent un peu de poids (3-5 kg en moyenne), mais paradoxalement leur sensibilité à l’insuline s’améliore nettement. Cela s’explique par une rétention d’eau et par le fait que la graisse est redirigée vers le tissu adipeux (stockage sûr) et quitte le foie et les muscles. On peut voir ce traitement comme “soignant le tissu adipeux” en augmentant sa capacité de stockage saine. Des études d’imagerie ont confirmé que la pioglitazone augmente la masse grasse sous-cutanée mais réduit la graisse hépatique et améliore la composition du tissu adipeux (adipocytes plus petits, plus d’adiponectine). Malheureusement, les TZD ont des effets secondaires (rétention d’eau, risque d’insuffisance cardiaque, etc.) qui limitent leur usage, et ils ne sont pas approuvés spécifiquement pour l’obésité sans diabète. Néanmoins, ils ont démontré le principe qu’on peut traiter l’obésité en augmentant la qualité du tissu adipeux plutôt qu’en le supprimant. C’est un changement de paradigme intéressant : au lieu de chercher à détruire la graisse, on la transforme en “bonne graisse” active et on la répartit mieux. Cela ne fait pas maigrir sur la balance, mais le patient va beaucoup mieux métaboliquement. À l’avenir, on pourrait imaginer des molécules plus ciblées qui exploitent ce concept sans les inconvénients des TZD.
Anti-inflammatoires : Étant donné le rôle de l’inflammation adipocytaire, des anti-inflammatoires ont été testés pour améliorer la sensibilité à l’insuline. Par exemple, la salsalate (un vieux salicylé) ou des inhibiteurs de JNK, mais les résultats cliniques sont modestes et non utilisés couramment. Des antagonistes de cytokines (anti-TNF, IL-1) n’ont pas montré d’amélioration suffisante du diabète pour justifier leur emploi (sauf peut-être l’IL-1 dans certains diabètes, mais c’est un cas particulier). Il est probable qu’une fois le processus établi, bloquer une cytokine ne suffit pas, car d’autres prennent le relais. Donc pas de “pilule anti-inflammatoire du tissu adipeux” pour l’instant. En revanche, les acides gras oméga-3 à haute dose ou certains flavonoïdes (comme la quercétine) sont étudiés pour leurs effets anti-inflammatoires sur le tissu adipeux : par exemple, une combinaison dasatinib+quercétine a été testée pour éliminer les cellules sénescentes (inflammatoires) du tissu. Mais c’est encore expérimental.
Agents modulant la fibrose : Il n’existe pas de médicament spécifique pour réduire la fibrose adipeuse. Certaines molécules comme la pirfénidone (antifibrotique utilisé dans la fibrose pulmonaire) pourraient théoriquement agir, mais elles ont des effets systémiques importants et pas d’indication dans l’obésité. La metformine a quelques propriétés anti-fibrotiques indirectes via l’AMPK et pourrait limiter la fibrose du tissu adipeux en améliorant l’oxygénation (elle favorise l’angiogenèse dans certains modèles). Mais ce n’est pas son effet principal.
En résumé, la pharmacologie récente s’est focalisée sur la réduction pondérale globale (GLP-1) et la redistribution métabolique (TZD). Les premiers ciblent l’axe cerveau (régulation de l’appétit), les seconds ciblent l’organe adipeux directement. L’avenir est peut-être de combiner les deux approches, ce qui arrive d’ailleurs : des nouvelles molécules “combinées” comme tirzepatide (agoniste dual GLP-1/GIP) provoquent une perte de poids encore plus importante (–20% dans des essais), ce qui va définitivement soulager le tissu adipeux de son excès. On peut imaginer qu’ensuite, on utilise un modulateur de PPAR-γ plus fin pour consolider la fonctionnalité du tissu adipeux restant.
Chirurgie bariatrique : C’est actuellement le traitement le plus efficace de l’obésité morbide. En restreignant drastiquement l’apport alimentaire (et/ou l’absorption), la chirurgie (Sleeve gastrectomie, Bypass gastrique, etc.) induit une perte de poids majeure (souvent >25% du poids initial). Cela se traduit par une fonte massive du tissu adipeux sur 12 à 18 mois. La chirurgie a aussi des effets hormonaux (augmentation du GLP-1 endogène, etc.) qui potentialisent la perte et maintiennent la satiété. D’un point de vue du tissu adipeux :
On observe après chirurgie une diminution spectaculaire de la taille des adipocytes et parfois même du nombre d’adipocytes (il peut y avoir un certain degré d’apoptose adipocytaire car la perte est rapide, et potentiellement une autophagie). Une régression de la stéatose hépatique (en quelques mois) et une amélioration de la sensibilité à l’insuline quasi immédiate (souvent avant même la grande perte de poids, grâce aux changements hormonaux). Une diminution de l’inflammation systémique (CRP, IL-6 chutent), et une hausse de l’adiponectine. Chez certaines patientes, l’hyperandrogénie du syndrome des ovaires polykystiques s’améliore, la fertilité revient, signe que l’axe gonadique ressent la diminution du tissu adipeux délétère.
À plus long terme, le tissu adipeux se reconstruit différemment : souvent la proportion de graisse viscérale est beaucoup plus faible après. La distribution peut redevenir quasi normale. Cependant, en cas de reprise de poids, on a remarqué que souvent c’est la graisse viscérale qui revient vite (peut-être parce que la structure fibreuse du TA viscéral initial reste et facilite un remplissage).
La chirurgie, en vidant le tissu adipeux, montre à quel point toutes les anomalies métaboliques peuvent s’améliorer jusqu’à disparaître chez un ex-obèse. Bien sûr, ce n’est proposé qu’aux obésités sévères ou compliquées, car la procédure est très invasive. Mais le message est : plus on peut décharger durablement le tissu adipeux, mieux c’est pour la santé globale.
Thérapies expérimentales : On peut en mentionner quelques-unes futuristes :
Transplantation de tissu adipeux brun : chez la souris, implanter de la graisse brune supplémentaire améliore le métabolisme. Chez l’homme, on n’en est pas là, mais on étudie comment différencier des cellules souches en adipocytes bruns et les greffer.
Génie génétique : cibler des gènes clés du tissu adipeux. Par exemple, une piste serait de bloquer la protéine de liaison au collagène VI (enzyme ATX) pour limiter la fibrose, ou de moduler HIF-1. Cependant, la crainte de l’effet inverse existe. Par exemple, la surexpression d’HIF-1 favorise l’obésité…
Cellules sénescentes : Avec l’âge, des adipocytes deviennent sénescents et sécrètent beaucoup de cytokines (SASP). Éliminer ces cellules par des sénolytiques (molécules qui tuent préférentiellement les cellules sénescentes) est exploré pour améliorer la fonction du tissu adipeux chez des personnes obèses âgées.
Microbiote : Le microbiote intestinal influence le stockage lipidique. Des transplantations fécales de donneurs maigres vers des obèses ont montré de légères améliorations de sensibilité à l’insuline. Le microbiote communique avec le tissu adipeux via des métabolites (acides gras à chaîne courte, etc.). Peut-être qu’agir sur le microbiote (prébiotiques, probiotiques) modulerait aussi la fonction adipocytaire. Par exemple, certains probiotiques réduisent l’inflammation adipocytaire dans certains modèles.
Appareils ou traitements locaux : La cryolipolyse détruit localement des adipocytes par le froid intense (dans un objectif esthétique), mais on peut se demander si enlever la graisse sous-cutanée par ce biais affecte la santé métabolique. La liposuccion chirurgicale retire aussi de la graisse, mais les études ont montré qu’enlever 5 kg de graisse sous-cutanée n’améliorait pas du tout les paramètres métaboliques car car la masse grasse viscérale n’est pas touchée, et la physiologie adipocytaire n’est pas modifiée. Parfois même, après liposuccion, le corps tend à regagner ce qui a été enlevé, parfois dans des dépôts plus profonds. Cela souligne qu’il faut traiter la cause (excès calorique) et la fonction adipocytaire, pas juste retirer la graisse superficielle.
Conclusion
Le tissu adipeux, autrefois perçu comme un simple rembourrage inerte et disgracieux, s’impose aujourd’hui comme un organe central de la physiologie dont la diversité, la plasticité et les dérèglements influencent profondément la santé humaine. Nous avons vu qu’il existe plusieurs types de graisses (blanche, brune, beige) aux fonctions complémentaires, et que la distribution anatomique des dépôts adipeux est un facteur clé, faisant souvent la différence entre un excès pondéral bien toléré et un excès délétère.
La plasticité du tissu adipeux permet à l’organisme de s’adapter aux fluctuations énergétiques : en stockant plus ou moins de lipides, en recrutant de nouveaux adipocytes, en modifiant la taille des cellules, voire en convertissant des adipocytes blancs en adipocytes bruns ou en remodelant sa vascularisation et son milieu immunitaire. Cette plasticité est le garant d’une expansion saine. Lorsqu’elle atteint ses limites (hypertrophie extrême, inflammation non résolue, fibrose rigide), le tissu adipeux entre en dysfonctionnement et devient le point de départ d’une cascade de troubles métaboliques (insulino-résistance, dyslipidémie, stéatose hépatique, etc.).
L’obésité peut être lue, d’un point de vue mécanistique, comme l’histoire d’un tissu adipeux d’abord trop sollicité puis débordé et malade. Par effet domino, un tissu adipeux malade envoie de mauvais signaux à l’organisme, qu’il s’agisse d’un cerveau trompé sur l’état des réserves, d’un foie engorgé par les graisses, d’artères enflammées ou d’un pancréas épuisé. Ainsi, la notion d’adiposopathie prend tout son sens : ce n’est pas tant la quantité de gras qui pose problème que la perte de sa fonctionnalité.
En pratique, ces connaissances se traduisent par un suivi du tour de taille, un changement profond des habitudes et des comportements alimentaires, un encouragement à l’activité physique, et par une prise de conscience qu’une modeste perte de poids peut apporter des bénéfices disproportionnés si elle vise le bon compartiment graisseux. On comprend aussi mieux certaines conditions comme l’obésité métaboliquement saine (le tissu adipeux parvient encore à gérer) ou inversement le diabète du sujet non obèse (tissu adipeux trop restreint ou défaillant). Cela appelle à une approche plus personnalisée du surpoids : traiter “la personne et son tissu adipeux”, plutôt qu’un chiffre d’IMC.
Pour conclure, le tissu adipeux est un organe endocrine et immunitaire dynamique, doué d’une étonnante faculté de remodelage, au cœur d’un équilibre subtil entre santé et maladie. S’il demeure flexible et bien régulé, il protège l’organisme des aléas énergétiques. Mais s’il se rigidifie et s’enflamme, il devient le foyer de pathologies systémiques. La bonne nouvelle est que, même lorsqu’il a été malmené, le tissu adipeux garde une capacité d’amélioration : en réduisant l’excès calorique, en mobilisant ses réserves par l’exercice, et grâce aux thérapies émergentes, on peut restaurer en partie ses fonctions. Autrement dit, l’histoire du tissu adipeux n’est pas figée. Cette notion porte un message d’espoir pour les patients : en s’attaquant aux causes (mode de vie, facteurs environnementaux) et avec les outils médicaux appropriés, il est possible d’inverser le cours du syndrome métabolique en donnant au tissu adipeux les moyens de revenir à un fonctionnement plus sain.
Le défi pour les années à venir sera de continuer à démêler les mécanismes intimes de cette plasticité adipocytaire, pour mettre au point des interventions encore plus ciblées et efficaces, comme stimuler sélectivement les tissus adipeux brun/beige, accroître la capacitié du tissu adipeux sans favoriser l’obésité, ou encore identifier des biomarqueurs circulants fiables de l’état de santé du tissu adipeux. Quoi qu’il en soit, reconnaître le tissu adipeux comme un organe clé doit être à la base du changement : on ne lutte pas (seulement) contre la graisse pour des raisons esthétiques, on prend soin d’un organe dont dépend en grande partie notre équilibre métabolique.
Références
- Arner, E., Westermark, P. O., Spalding, K. L., Britton, T., Rydén, M., Frisén, J., Bernard, S., & Arner, P. (2010). Adipocyte Turnover: Relevance to Human Adipose Tissue Morphology. Diabetes, 59(1), 105–109.
- Cypess, A. M., Lehman, S., Williams, G., Tal, I., Rodman, D., Goldfine, A. B., Kuo, F. C., Palmer, E. L., Tseng, Y.-H., Doria, A., Kolodny, G. M., & Kahn, C. R. (2009). Identification and Importance of Brown Adipose Tissue in Adult Humans. New England Journal of Medicine, 360(15), 1509–1517.
- De Fano, M., Bartolini, D., Tortoioli, C., Vermigli, C., Malara, M., Galli, F., & Murdolo, G. (2022). Adipose Tissue Plasticity in Response to Pathophysiological Cues: A Connecting Link between Obesity and Its Associated Comorbidities. International Journal of Molecular Sciences, 23(10), 5511.
- Gilani, A., Stoll, L., Homan, E. A., & Lo, J. C. (2024). Adipose Signals Regulating Distal Organ Health and Disease. Diabetes, 73(2), 169–177.
- Liu, F., He, J., Wang, H., Zhu, D., & Bi, Y. (2020). Adipose Morphology: A Critical Factor in Regulation of Human Metabolic Diseases and Adipose Tissue Dysfunction. Obesity Surgery, 30(12), 5086–5100.
- Lopez-Yus, M., Hörndler, C., Borlan, S., Bernal-Monterde, V., & Arbones-Mainar, J. M. (2024). Unraveling Adipose Tissue Dysfunction: Molecular Mechanisms, Novel Biomarkers, and Therapeutic Targets for Liver Fat Deposition. Cells, 13(5), 380.
- Mo, Y.-Y., Han, Y.-X., Xu, S.-N., Jiang, H.-L., Wu, H.-X., Cai, J.-M., Li, L., Bu, Y.-H., Xiao, F., Liang, H.-D., Wen, Y., Liu, Y.-Z., Yin, Y.-L., & Zhou, H.-D. (2024). Adipose Tissue Plasticity: A Comprehensive Definition and Multidimensional Insight. Biomolecules, 14(10), 1223.
- Peirce, V., Pellegrinelli, V., & Vidal-Puig, A. (2016). Adipose Structure (White, Brown, Beige). In R. S. Ahima (Ed.), Metabolic Syndrome (pp. 369–396). Springer International Publishing.
- Peng, Y., Zhao, L., Li, M., Liu, Y., Shi, Y., & Zhang, J. (2024). Plasticity of Adipose Tissues: Interconversion among White, Brown, and Beige Fat and Its Role in Energy Homeostasis. Biomolecules, 14(4), 483.
- Rutkowski, J. M., Stern, J. H., & Scherer, P. E. (2015). The cell biology of fat expansion. Journal of Cell Biology, 208(5), 501–512.
- Saito, M., Okamatsu-Ogura, Y., Matsushita, M., Watanabe, K., Yoneshiro, T., Nio-Kobayashi, J., Iwanaga, T., Miyagawa, M., Kameya, T., Nakada, K., Kawai, Y., & Tsujisaki, M. (2009). High Incidence of Metabolically Active Brown Adipose Tissue in Healthy Adult Humans. Diabetes, 58(7), 1526–1531.
- Sakers, A., De Siqueira, M. K., Seale, P., & Villanueva, C. J. (2022). Adipose-tissue plasticity in health and disease. Cell, 185(3), 419–446.
- Stenkula, K. G., & Erlanson-Albertsson, C. (2018). Adipose cell size: Importance in health and disease. American Journal of Physiology-Regulatory, Integrative and Comparative Physiology, 315(2), R284–R295.
- Virtanen, K. A., Lidell, M. E., Orava, J., Heglind, M., Westergren, R., Niemi, T., Taittonen, M., Laine, J., Savisto, N.-J., Enerbäck, S., & Nuutila, P. (2009). Functional Brown Adipose Tissue in Healthy Adults. New England Journal of Medicine, 360(15), 1518–1525.
- Weisberg, S. P., McCann, D., Desai, M., Rosenbaum, M., Leibel, R. L., & Ferrante, A. W. (2003). Obesity is associated with macrophage accumulation in adipose tissue. Journal of Clinical Investigation, 112(12), 1796–1808.
- Zwick, R. K., Guerrero-Juarez, C. F., Horsley, V., & Plikus, M. V. (2018). Anatomical, Physiological, and Functional Diversity of Adipose Tissue. Cell Metabolism, 27(1), 68–83.